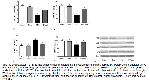
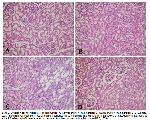
Mevcut araştırmada, taurinin STZ ile diyabet oluşturulan ratların böbrek dokusunda PPARγ, IRS-1, HSP-27 ve HSP-72 proteinlerinin düzeyleri üzerine etkisi araştırılmış ve gruplar arasında anlamlı farklılık tespit edilmiştir. Taurin uygulanmış gruplarda PPARγ, IRS-1, HSP-27 ve HSP-72 düzeylerinde kontrol grubuna göre anlamlı bir değişim görülmezken, STZ uygulanmış gruplarda PPARγ, IRS-1 ve HSP-72 düzeylerinde anlamlı bir düşüş gerçekleştiği görülmüştür. Ancak, HSP-27 düzeyinde STZ uygulanmış grupta belirgin bir artış gözlenmiştir. Aynı şekilde, STZ+Taurin uygulanmış gruplarda PPARγ, IRS-1 ve HSP-72 düzeylerinde STZ uygulanmış gruplara göre artış olduğu tespit edilirken, HSP-27 düzeyinde düşüş olduğu belirlenmiştir. Bu sonuçlara göre, STZ ile diyabetik nefropati oluşturulan ratlarda taurin uygulanmasının nefropatiyi yavaşlatıcı ve iyileştirici etkisinin olduğu söylenebilir.
Diyabet, insülin direnci veya eksikliği nedeniyle oluşur ve kontrol edilmeyen diyabet genellikle retinopati, nöropati, nefropati, kardiyomiyopati, koroner arter hastalığı, periferik arter hastalığı ve felçin dahil olduğu mikrovasküler ve makrovasküler komplikasyonların artış riskiyle birlikte ciddi komplikasyonlara neden olur 19. STZ, muhtemelen aşırı reaktif oksijen türlerinin (ROS) üretimiyle pankreas β-hücrelerini yok ederek diyabete neden olur. Yapılan çalışmalarda, STZ-diyabetik ratlarda normal ratla kıyaslandığında açlık kan şekerinde önemli bir artış olduğu 20 ve iskelet kaslarınında etkilendiği gözlemlenmiştir 21. Ayrıca, mezengiyal hücrelerin genişlemesi, hücre dışı matriks protein birikimi, glomeruler ve tübüler bazal membran kalınlaşması, tubulointerstisyel fibrozis, glomeruloskleroz ve renal endotelyal disfonksiyon gibi patolojik değişikliklerin STZ-diyabetik ratların böbreklerinde oluştuğu belirtilmiştir 19,22.
Diyabette, oksidatif stresi artıran mekanizmaların başında, antioksidan savunma sisteminde meydana gelen aksaklıklar yer almaktadır. Serbest radikal oluşumunun diyabet ile birlikte artması ve bunun bir sonucu olarak gelişen radikal bağlayıcılarının azalması ile diyabette antioksidanlara daha çok ihtiyaç duyulduğu bildirilmiştir 23. Oksidatif stresin olumsuz etkilerini gidermek için diyetsel manüplasyonların uygulandığı çeşitli çalışmalar bulunmaktadır. Bu anlamda vitaminler, karotenoidler, mineral maddeler, biyoaktif bileşikler ve aminoasitler gibi moleküllerin kullanılabildiği bildirilmektedir 2,23.
Taurin; beyin, kalp, böbrekler ve üreme organları dahil birçok organda yüksek konsantrasyonlarda bulunur 24,25. Biyolojik sistemlerdeki antioksidan olarak taurinin başlıca faydalı etkileri; ROS temizlemek, biyomembranların bütünlüğünü korumak ve lipid peroksidasyonunu azaltmak şeklinde ortaya çıkar 26. Taurinin hipoglisemik etkisini, insülinin etkisini ve insulinle reseptörünün etkileşimini artırarak gösterdiği belirlenmiştir 14. Plazmadaki taurin düzeyleri beta hücreleri ve insülin aktivitesi için önemlidir 27. Ribeiro ve ark. 28 tarafından yapılan bir çalışmada hayvanların içme suyuna 30 gün boyunca yüzde 2 oranında taurin eklenmiş ve taurin alan grubun kontrol grubuna göre glukoz toleransında ve yüksek oranda insülin duyarlılığında düzelme olduğu bildirilmiştir. Gavrovskaya ve ark. 29, taurin uygulamasıyla, insülin hassasiyetinin düzeldiğini ve taurinin glukoz metabolizmasındaki enzimleri onarmasının yanı sıra, fruktozla beslenmiş ratlarda hiperglisemi ve hiperinsülinemiyi kontrol altına aldığı gösterilmiştir. Winiarska ve ark. 13 tarafından yapılan çalışmada, taurin tedavisinin diyabetle sitimule edilen renal NADPH oksidaz aktivitesini normale döndürebildiği ayrıca diyabete özgü olan hem albuminüri hem de glomerulopatiyi hafiflettiğini bildirmişlerdir. Higo ve ark. 30, diyabetik ratlarda taurin alımının proteinuri gelişimi ve mezengial ekstraselular matriks genişlemesinin azalttığını bildirmişlerdir 13,30. Bu çalışmalar 13,27-30 ile mevcut araştırmadaki sonuçlarla taurinin hem diyabet hem de nefropatinin tedavisinde yararlı olduğu ayrıca bu sonuçların taurinin antioksidan etkileri vasıtasıyla diyabetik nefropati gelişimini baskılayabildiği öngörülmektedir.
IRS-1, IRS protein substrat ailesinin bir üyesidir. İnsülin sinyallerinde önemli bir rol oynadığı düşünülmektedir 31,32. IRS-1 geninin kodon 972de (Gly972Arg) bulunan arjinine bir glisin eklenmesinin insülin direnci ve bozulan insülin salgılanması nedeniyle tip 2 diyabetin yüksek prevalansı ile ilişkili olduğu gösterilmiştir 32. IRS-1, insülin reseptörünün tirozin kinaz aktivitesi için önemli bir substrattır. Nitekim, IRS-1in diyabetli hastalar ve hayvanlar ile obez bireylerde azaldığı bulunmuştur 33. Sahin ve ark. 34, STZ, krom pikolinat (CrPic) ile biotinin IRS-1 ekspresyon düzeyleri üzerindeki etkilerine yönelik yaptıkları çalışmalarında, yüksek yağlı diyetle beslenen ve STZ uygulanan grupta, karaciğer, böbrek ve kas dokularında azalma, CrPic, STZ ve biotinin ayrı ayrı ve birlikte uygulandığı gruplarda ise artış olduğu gözlenmiştir. Yapılan bu çalışmalardaki 33,34 sonuçlarla mevcut araştırmamızdaki IRS-1 düzeyinin, STZ uygulanmış gruplarda düşmesi, STZ+Taurin uygulanan gruplarda artması bulguları paralellik göstermektedir.
Diyabetik nefropatili hastalardaki yüksek HSP-27 seviyeleri, diyabetik nefropatiyle ilişkilidir. HSP-27 diyabetik nefropatinin erken teşhisinde de bir belirteç olabilir 35. Barutta ve ark. 36, diyabet ve ilişkili hastalıkların HSP-27, HSP-60 ve HSP-70in ekspresyonlarını ve fosforilasyonlarını etkilediklerini ve bununda renal hücrelerin sitoprotektif cevabını etkileyebileceğini rapor etmişlerdir. Oksidatif stresle ilişkili hipergliseminin tip 1 diyabetin vasküler komplikasyonlarının nedeni olabileceği ileri sürülmüştür 37, ve daha önceki bir çalışmada ise serum HSP-27 düzeyleri tip1 diyabetli hastalarda distal simetrik polinöropatiyle bağımsız olarak ilişkilendirilmiştir 38. Buna rağmen aynı hasta grubunda HSP-27 antikor düzeylerinin antijen varlığıyla uyumlu bulunmamıştır 39. Mevcut araştırmada, HSP-27 düzeyi STZ uygulanmış gruplarda artmış ve STZ+taurin uygulanan gruplarda ise düşmüş olduğu sonucu yukarıdaki çalışmaların sonucu ile desteklenmiştir.
Diyabetik memelilerde yapısal HSP ekspresyonunun azaldığını ya da değişmediğini bildiren çalışmalar vardır 40,41. Diyabetik ratlardaki karaciğer ve adrenal bezlerdeki ısıyla eksprese edilen HSP72 ekspresyonunun önemli ölçüde düştüğü rapor edilmiştir 41. Buna ek olarak, ısı stresinden sonra oluşan miyokardiyal HSP72 miktarının diyabetik ve non diyabetiklerde benzer olduğu gösterilmiştir 42. Gençoğlu 43nun beyin ısı şok proteini 70 (Hsp-70) ekspresyon düzeylerine yönelik yaptığı çalışmasında, yüksek yağlı diyetle beslenen ve STZ uygulanan ratlarda, krom histidinatın belirgin bir şekilde ısı şok protein ekspresyonlarında gerileme sağlayabildiği tespit edilmiştir. Kavanagh ve ark. 44, yaptıkları çalışmalarında HSP-70 proteinlerinin, tip 2 diyabetli primatların dolaşımında azaldığını belirlemişlerdir. Atalay ve ark. 45, ise diyabetik ratlarda HSP-72nin kalp ve karaciğer kaslarında düşük bulunduğu, fakat gastrocnemius kasında değişmediğini bildirmişlerdir. Bu çalışmada HSP-72 düzeyi STZ uygulanmış gruplarda azalmış ve STZ+taurin uygulanan gruplarda ise artış göstermiştir.
Çok sayıda deneysel ve klinik çalışmalar, diyabetik nefropatinin gelişimini önlemede PPAR-γ agonistlerinin tedavi edici potansiyelini göstermiştir 19,46. Sahin ve ark. 34, STZ, krom pikolinat (CrPic) ile biotinin PPARγ ekspresyon düzeyleri üzerine etkileri ile ilgili çalışmalarında, yüksek yağlı diyetle beslenen ve STZ uygulanan grupta PPAR-γnın yağ dokusunda azaldığını göstermiştir. Kanie ve ark. 47, yaptıkları çalışmalarında, PPARγ ekspresyonun, STZ uygulanarak oluşturulan diyabetik ratlarda azaldığını belirlemişlerdir. Nicholas ve ark. 46, PPARγ ligandlarının mikroalbuminurinin azalmasında doğrudan rolü ve diabetik nefropatide tedavi edici özelliğinin olduğunu tespit etmişlerdir. Bütün bu çalışmalardaki PPARγnın iyileştirici özelliği sonucu ile mevcut çalışmanın sonucu örtüşmektedir.
Sonuç olarak, STZ ile diyabet oluşturulan ratların böbrek dokularında taurinin PPARγ, IRS-1, HSP-27 ve HSP-72 proteinlerinin düzeyleri üzerinde olumlu etkilerinin olduğu belirlenmiştir. Taurin uygulaması ile böreklerde diyabet etkisiyle oluşan histopatolojik değişikliklerin şiddetinin azaldığı görülmüştür. Elde ettiğimiz bulgulara göre, diyabetik ratlarda taurin uygulamasının böbrek hasarında yavaşlatıcı ve iyileştirici etkisinin olduğu söylenebilir.