Bor, insan ve hayvan biyolojisi için temel öneme sahip bir iz element olduğundan borun önemi giderek artmaktadır. Bor genellikle deri, beyin, sindirim, iskelet, bağışıklık olmak üzere vücudun çeşitli organlarını ve sistemlerini etkilemektedir. Ayrıca kemik oluşumunda rol oynayan kalsiyum, D vitamini ve magnezyum ile de etkileşim halindedir
1. Bu nedenle boratlar endüstriyel ölçekteki ilaçlarda, çoğunlukla boraks ve borik asitli farklı sıvılarda gıda takviyesi ve farklı gıda ürünlerinde de koruyucu olarak kullanılmaktadır. Bor, başta İngiltere olmak üzere Avrupa ülkelerinde, mineral ve multivitamin takviyesi olarak kullanılmasının yanısıra bazı gıdalarda esnekliği ve görünümü arttırmak için tekstür geliştirici olarak da kullanılmaktadır. Borik asit ve disodyum oktaborat tetrahidratın bazı bakteri suşları üzerine antibakteriyel ve antibiyofilm etkiler gösterdiği bildirilmektedir. Antimikrobiyel ajanlardan borik asit ve tuzlarını içeren jelatinden antimikrobiyel ve biyobozunur gıda ambalaj malzemelerinin geliştirilmesi yönünde de çalışmalar mevcuttur.
1. Bor
Bor, simgesi B, atom numarası 5, atom ağırlığı 10.81 g/mol olan, periyodik cetvelde 3A grubunda yer alan, metalik ve ametalik özellik gösteren bir elementtir. Bor, doğada elementsel bir form olarak oluşmaz, kimyası karmaşıktır ve diğer elementlerle bileşikler (boratlar) oluşturur 2. Bor, Amerika Birleşik Devletleri (ABD)'nin batısı, Türkiye, Brezilya, Rusya ve Çin'in bazı bölgelerinde yüksek miktarda bulunmaktadır 2,3. Türkiyenin dünya bor rezervinin yaklaşık %73üne 4 sahip olması ve bor bileşiklerinin kullanım alanlarının geniş olması ülkemizin stratejik önemini arttırmaktadır.
Tabiatta yaklaşık 230 çeşidi olan bor mineralinin, oksijenle bağ yapmaya yatkın olması sebebiyle çok sayıda bor-oksijen bileşimi bulunmaktadır. Bor-oksit bileşiklerinin genel adı borattır 5. Ayrıca borun Ca, Mg ve sodyum elementleri ile de bileşikleri mevcut olup önemli olanlarından bazıları; boraks (Na2B4O7.10H2O), kolemanit (Ca2B6O11.5H2O) ve üleksittir (NaCaB5O9.8H2O). Bu bileşikler tabii boratlar olarak da bilinmektedir 6. Bor elementi 8B, 10B, 11B, 12B, 13B izotoplarından oluşmaktadır. En kararlı izotopları 10B ve 11Bdir. Bu izotopların tabiatta bulunma oranları sırasıyla %19.1-20.3 ve %79.7-80.9'dir 5. Bor, borik asit ve borat bileşikleri şeklinde insanlar tarafından binlerce yıl biyomedikal amaçla kullanılmasına rağmen 7, ilk gıda koruyucusu olarak 1870'lerde kullanılmıştır. Ayrıca borat ilavesi, et ve süt ürünleri gibi gıdaların lezzetini korumak veya raf ömrünü uzatma yöntemlerinden biri olarak kabul edilmiştir 8. Borun, insan ve hayvan metabolizmasına katkıda bulunduğu da bilinmektedir. Borun biyolojik etkileri, canlı organizmaların biyolojik sistemleri üzerindeki metabolik etkilerine de bağlanabilir. Canlı organizmalarda bor birçok enzimi, kemik gelişimini, mineralizasyonu, kalsiyum, fosfor, magnezyum ve enerji metabolizmasını etkilemektedir 9.
2. Bor ve Et Kalitesi
Et kalitesinin en önemli göstergelerinden bazıları pH, kül içeriği ve et rengidir 10. Etin pH değerindeki değişiklik etin kalitesini önemli ölçüde etkilemektedir. Bu durum kesimden önce kas glikojen depolarındaki değişikliklerin doğrudan bir sonucudur 11. Yüksek pH'da protein, suyla daha kuvvetli bir şekilde bağlanarak daha az serbest su ve daha koyu bir et rengi elde edilebilmektedir 12. Ayrıca yüksek pH'da, etin lezzet bileşenlerinden hassasiyet artmakta ve lezzet daha az olmaktadır 11. Bor, oksidoredüktazların yardımıyla spesifik metabolik yollarla ilişkili süreçlerin kontrolünde temel bir rol oynamaktadır. Oksidoredüktazlar, enzim aktivitesini teşvik etmek için piridin nükleotidine ihtiyaç duyarlar. Bor, geçiş durumu analogları yaparak veya glikolizin önemli substratları olan nikotinamid adenin dinükleotid (NAD) veya flavin adenin dinükleotid (FAD) için rekabet ederek bu enzimlerin aktivitesini tersine çevirir 13. Bor, NAD'ye etki ederek glikolitik yolu inhibe etmekte böylece kasın laktik asit içeriğini azaltarak pH değerini etkilemektedir 14. Ayrıca borik asidin yüksek dozlarının (3.4 ve 4.5 mmol B/kg CA) tavuk göğüs kaslarında metabolit (örneğin; glikoz, glikojen, laktat ve ATP) azalmasına neden olarak kasın pH değerini yükselttiği bildirilmiştir 15. Kastaki kül içeriği de etin içindeki mineralleri ve eser elementleri temsil ettiği için önemli bir indekstir 16. Bor; magnezyum, fosfor, molibden ve kalsiyum gibi minerallerin metabolizması üzerine faydalı etkilere sahiptir 17. Etlik piliçlerin içme suyuna ilave edilen borun (100 mg/L) aynı zamanda etteki demir ve çinko seviyelerini de arttırdığı bildirilmiştir 18. Bor, kasın mineral içeriğini etkili bir şekilde arttırdığından kül içeriği kademeli bir artış gösterir fakat bor ve kül miktarı arasındaki bu ilişkiyi belirlemek için daha fazla araştırmaya ihtiyaç vardır.
Bor takviyesi ayrıca serin proteazların aktivitesini de inhibe etmektedir. Serin proteazlar, prekürsör proteinlerin aktivasyonu ile çeşitli fizyolojik süreçlerde rol oynayan en bol proteolitik enzim gruplarından birini içermektedir 19. Yapılan bir çalışmada 14, devekuşu etinin fiziksel ve kimyasal özelliklerini değerlendirmek için devekuşlarının içme suyuna farklı dozlarda (160, 320 ve 640 mg/L) bor verilmiştir. Etin fiziksel özellikleri (örneğin; pH, damlama kaybı, pişirme kaybı), bor verilmesini takiben önemli sonuçlar göstermiştir. Bor ilavesi ile pişirme kaybının ve damlama kaybının azaldığı, et renginin ise etkilenmediği ortaya konmuştur. Devekuşu etinin kimyasal özellikleri değerlendirildiğinde (örn., nem, yağ, protein, kül ve kolesterol seviyeleri) bor ile işlem görmüş grupların, bor ile işlem görmemiş gruplara kıyasla protein ve kül değerleri anlamlı çıkmıştır. Devekuşu civcivlerinde etin hem fiziksel hem de kimyasal özelliklerinde 160 mg/L'ye kadar olan bor dozları etkili bulunmuştur.
3. Gıdalarda Bor Düzeyleri ve Gıda Takviyelerinde Bor Uygulamalari
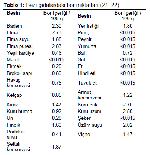
Bor, gıdalarda bulunabilen ve doğrudan toprak minerallerinden elde edilebilen bir mineraldir. Literatür araştırmalarına göre bor içeriği zengin gıdalar kabuklu yemişler, kuru baklagiller (1.0-4.5 mg/100 g), meyve ve sebzelerdir (0.1-0.6 mg/100 g). Borun tahıllarda ve patateste az miktarda olduğu belirtilmektedir. Et ve et ürünleri, süt ve süt ürünleri ve yumurta (<0.06 mg/100 g) ise bor açısından fakir gıdalardır 20. Bazı gıdalardaki bor miktarları Tablo 1de gösterilmiştir 21,22.
Bor bileşikleri, ticari olarak kullanılmakta olup neredeyse borun tamamı bor-oksijen bileşikleri halinde bulunmaktadır. Bordaki ester bağlarının oluşumu sayesinde bor ticari uygulamalarda kullanılma olanağı bulmuş ve bu durum borun biyolojik etkileşimi için bir temel oluşturmuştur. Boratlar çoğunlukla kapsüllerde, efervesan tozlarda, çiğnenebilir tabletlerde, boraks ve borik asitli farklı sıvılarda gıda takviyesi olarak kullanılmaktadır. Bu ürünlerin formülasyonları farklı ürünlerde değişir. Ayrıca bu boratlar farklı gıda ürünlerinde 4 g/kg dozunda koruyucu olarak da kullanılabilir 23. Amerika Gıda Takviyesi Veri Tabanına göre 2357 farklı gıda takviyesinde bor mevcut olup gıda endüstrisinde; kalsiyum fruktoborat, bor sitrat, bor aspartat, bor glisinat şelatları, bor askorbat ve sodyum borat içeren ürünler bulunmaktadır 24. Örneğin piyasada bor sitrat içeren Solgar Calcium Magnesium Plus Boron ve sodyum borat içeren Holland&Barrett Boron isimli ürünler bulunmaktadır.
Borik asit ve disodyum oktaborat tetrahidrat, bazı bakteri suşları üzerinde (Staphylococcus aureus ATCC 25923, Aeromonas hydrophila ATCC 19570, Brucella melitensis Rev1, Vibrio anguillarum, Aeromonas hydrophila, Yersinia ruckeri, Brucella abortus) antibakteriyel ve antibiyofilm etkiler göstermiştir. Borun bu etkisi tıp ve endüstride farklı fonksiyonel mikroorganizmalarda yeni yöntemler ile kullanılması açısından önemlidir 25. Borun biyolojik sistemlerdeki önemli rolünün farkındalığı son yıllarda ortaya çıkmıştır. Birçok ülkede boratların gıda ürünlerinde kullanımına izin verilmiştir 26. Bor karides, erişte, pirinç ve nişasta jölesi gibi bazı gıdalarda esnekliği ve canlılığı arttırmak için bir tekstüre ajan olarak kullanılır. Avustralya Terapötik Ürünler İdaresi Başkanlığı kendi ülkelerinde 14 oral borat diyet takviyesi için lisans vermiştir. Ayrıca takviye konsantrasyonunun günde 3 mg'den az olması gerektiğini belirtmiştir. Bu takviyeler çoğunlukla D vitamini, magnezyum ve kalsiyum kombinasyonunda kullanılır 27. Borat kullanımı İngiltere ve Avrupa ülkelerinde mineral ve multivitamin takviyesi olarak yaygın bir şekilde kullanılmaktadır. Boratların ticari ölçekte tek sınırlaması güvenli miktarda olması gereken konsantrasyonudur. 2004 yılında, Avrupa Gıda Güvenliği Otoritesi (EFSA), yaş gruplarına bağlı olarak bor tüketimi için tolere edilebilir üst seviye miktarını 3-10 mg/gün olarak belirlemiştir 28. Bu nedenle yukarıda belirtilen üst seviyenin aşılmaması durumunda boratlar (özellikle sodyum borat ve borik asit), gıda maddelerine ve diyetlere spesifik beslenme amaçları doğrultusunda takviye için uygundur.
Liu ve ark. 29, pH değişikliklerini izleyebilen ve gıdalarda istenmeyen mikrobiyel büyümeyi önleyebilen akıllı bir nişasta/poli-vinil alkol (PVA) filmi geliştirmişlerdir. Filmdeki nişasta ve PVA polimerleri, suya dayanıklıklarını ve mekanik güçlerini arttırmak için iki kez sodyum trimetafosfat ve borik asit ile çapraz bağlanmıştır. Bor bileşiklerinin gıda ambalaj malzemelerinde kullanılması yönünde çalışmalar yapılmaya başlanmıştır. Argın ve ark. 30, yapmış oldukları çalışmada, antimikrobiyel ajan olarak borik asit (H3B03) ve tuzlarını (disodyum oktaborat tetrahidrat: Na2B8O13.4H20; sodyum pentaborat: NaB5O15) içeren jelatinden antimikrobiyel ve biyobozunur ambalaj malzemeleri geliştirmişlerdir.
4. Bora Maruz Kalma Yolları ve Toksik Etkileri
Bor toprakta ortalama 5-150 mg/kg, yer kabuğunda 10 mg/kg, deniz suyunda 4.6 mg/L ve havada ise 20 ng/m3 miktarda bulunmaktadır 20. Bor, vücuda başlıca gıdalar ve içme suyu ile alınmaktadır. Bor madeninin üretildiği ve/veya işlendiği yerlerde ayrıca sabun, deterjan ve kozmetik ürünlerin üretildiği yerlerde çalışan ve/veya bu ürünleri kullanan kişiler bor bileşiklerine solunum yoluyla veya deri ile temas yoluyla maruz kalmaktadır 31.
Bor ve bor bileşiklerinin vücut üzerindeki toksik etkileri özellikle doku düzeyinde yeterince çalışılmamıştır. Ancak Beyin-omurilik zarında tıkanıklık, yangı, eksfolyatif dermatit, böbrek epitel hücrelerinin dejenerasyonu, şişme ve ödeme neden olduğu bildirilmiştir. Diyet veya sudaki seviyesine ilişkin risk değerlendirmelerinde, sodyum borat ve borik asidin yüksek düzeyde toksisiteye neden olduğunu göstermiştir. Sudaki sodyum borat ve borik asit, deri yanmasına neden olmaz fakat gözlerde tahrişe neden olmaktadır 32. Bor bileşikleri, test edilen tüm türlerde yüksek dozlarda zehirlidir fakat kanserojenik ya da mutajenik değildir. Ana toksisiteler reprodüktif ve gelişimsel olmaktadır 33. Borik asit için en düşük ölüm dozu insanlar tarafından ağız yolu ile alındığında 640 mg/kg, deri yolu ile alındığında 8600 mg/kg, enjeksiyon yolu ile alındığında 29 mg/kg, total doz ise, erişkinler için 5-20 g, çocuklar için 5 gramın altı olarak bildirilmiştir. Günde toplam 500 mgdan fazla bor alınması durumunda insanlarda bulantı, kusma, baş ağrısı, karın ağrısı, ishal, kas kasılması, şok, halsizlik, sindirim ve merkezi sinir sistemi düzensizlikleri, salgı bezlerinin çalışmasının bozulması ve cilt lezyonları gibi toksisite belirtileri görülmektedir 32. Ancak gıdalar ile alınan bor miktarına bakıldığında insan ve hayvanlarda belirtilen bu dozu aşmanın mümkün olamayacağı da ifade edilmektedir 34.
5. Borun Günlük Alım Miktarı ve Tolere Edilebilir Üst Seviyesi
Dünya Sağlık Örgütüne (WHO) göre, içme suyundaki bor miktarı 0.1- 0.3 mg/L arasında olup ayrıca WHO tarafından gıda ile bor alımı yaklaşık 1.2 mg/gün olarak belirlenmiştir 32. ABD Tıp Enstitüsü Gıda ve Beslenme Kurulu yetişkinler için tolere edilebilir üst seviyeyi 20 mg/gün olarak belirlemiştir 35. WHO borun güvenli üst alım seviyesini ilk olarak 13 mg/gün olarak belirlemiş fakat daha sonra bu değeri artırarak 0.4 mg/kg olarak belirlemiştir 31. EFSA tarafından tolere edilebilir üst alım seviyesi toplam 10 mg/kg/gün olarak bildirilmiştir. EFSA panelinde bor için kabul edilebilir günlük alım miktarı 0.16 mg/kg/gün olarak belirlenmiştir 36. Avustralyada yapılan bir çalışmada kişilerin diyetle aldıkları bor miktarı ortalama 2.23±1.23 mg/gün olarak tespit edilmiştir 37. Gıdalar ve su ile bor alımı coğrafik koşullar ve diyet özelliklerine göre değişmekte ve bor alımının günlük toplam 1-7 mg olduğu ifade edilmektedir 38. EFSA verilerine göre ise içme suları ile günlük alınabilecek bor miktarının 0.2-0.6 mg/gün düzeyinde olabileceği bildirilmektedir 28.
6. Bor ve Antimikrobiyel Aktivitesi
Bor, çeşitli biyolojik işlevler gerçekleştiren tüm canlı organizmaların bileşenlerinde bulunur. Bor, borofisin, aplazmomisin, tartrolon ve boromisin 39 gibi antibiyotiklerin bir bileşeni olup bakteriyel quorum sensing sinyal molekülünde, oto-indükleyicide (AI-2) 40 ve vibrioferrinde bulunur. Boraks, (Na2B4O7.10H2O) en basit bor tuzlarından biri olup bu molekül aynı zamanda çok geniş bir homeopatik, antiseptik ve bakterisid etkilere sahiptir 41. Guhl 42, yaptığı araştırmada boratların, konsantrasyonlara bağlı olarak Pseudomonas putida, Photobacterium phosphoreum, Entosiphon sulcatum ve Paramecium caudatum gibi mikroorganizmaların gelişimlerini inhibe ettiğini gözlemlemiştir. Bowen ve Gauch 43, yapmış oldukları araştırmalarda, borun bazı mantar türlerinin (Saccharomyces cerevisiae, Neurospora crassa, Aspergillus niger ve Penicillum chrysogenum) gelişimlerinini inhibe etiiğini ve bu türler için esansiyel olmadığı sonucuna ulaşmışlardır. Bor bileşiklerinin su kaynaklarında Pseudomonas aeruginosa ATCC-27853 ve Escherichia coli MG1655/K12 tarafından üretilen biyofilmlerin inhibisyonu üzerine etkilerinin incelendiği bir çalışmada, 25 mg/mL sodyum tetraborat dekahidrat (STD) ve disodyum oktaborat tetrahidrat (DOT) konsantrasyonun test edilen bakteriyel biyofilm oluşumu üzerinde en etkili inhibisyona neden olduğu saptanmıştır 44. Bor türevlerinin diğer bir belirgin özelliği, E. coli, Klebsiella spp, Acinetobacter calcoaceticus, Enterobacter spp, Staphylococcus spp, Morganella spp, Proteus spp, Pseudomonas aeruginosa, Citrobacter spp ve benzeri gibi geniş mikroorganizmalar üzerindeki biyosidal etkisidir 45. Bazı durumlarda borik asit Candida spp enfeksiyonlarında 46, maya enfeksiyonlarında 47 ve antikandidal olarak 48 kullanılmıştır. Borik asidin 1969'da ilk bakteriyostatik etkileri bildirilmiştir 49. Böylece, borik asidin dezenfektanlar, böcek ilaçları ve bakteriyel hastalıkları tedavi etmek için umut verici bir antibakteriyel faktör olduğu anlaşılmaktadır 44. Bor, çeşitli mikroorganizmalara karşı 1950lerin ortalarına kadar antimikrobiyel gıda koruyucusu olarak kullanılmıştır. Günümüzde de klinik amaçlar için antifungal ajan olarak kullanılmaktadır 50. Demirci ve ark. 51, yaptıkları çalışmada bor türevlerinden borik asit ve sodyum pentaborat pentahidrat (NaB)ın in vitro koşullardaki antimikrobiyel etkinliklerini, deri hücreleri üzerindeki proliferasyon, migrasyon, anjiyogenez, gen ve büyüme faktörü düzeylerini arttırıcı etkilerini incelemişlerdir. Sonuçlar, her iki bor bileşiğinin de bakteri, maya ve mantarlara karşı önemli ölçüde antimikrobiyel etkilerinin varlığının yanı sıra, deri hücrelerinin proliferasyonunu, migrasyonunu, önemli gen ve büyüme faktörü düzeyini arttırdığını fakat NaBnin etkisinin daha fazla olduğunu tespit etmiştir.
Bakteriyel quorum sensing, biyofilm oluşumu ve bakteriyel virülens faktörlerinin üretimi gibi çeşitli biyolojik proseslerle ilişkili olduğundan bu sistemi inhibe edebilecek veya bozabilecek moleküllerin araştırılması önem taşımaktadır 52. Ni ve ark. 53, borik asit türevi moleküllerin quorum sensing üzerine inhibitör etkili antibakteriyel ajan olarak kullanılabileceklerini belirtmişlerdir. Biyofilm inhibisyonu ile ilgili yapılan bir çalışmada borik asitin insan oral kavitesinde Enterococcus feacalis tarafından oluşturulan biyofilm üzerine inhibitör etkili olabildiği ve irrigasyon sıvısı olarak kullanılabileceği belirtilmiştir 54. Argın ve ark. 30, yapmış oldukları çalışmada borik asit ve tuzlarını içeren jelatin filmler, Staphylococcus aureus ve Pseudomonas aeruginosa'ya karşı antibakteriyel etkinin yanı sıra, Aspergillus niger ve Candida albicans'a karşı gösterdiğini bildirmişlerdir. Raimondi ve ark. 55, borun farklı türevlerinin in vitro şartlada S. aureus ATCC 25923, E. coli ATCC 25922, C. albicans ATCC 10231 üzerine bakterisid ve fungisid etkiye sahip olduğunu bildirmişlerdir. Yilmaz 49, in vitro şartlarda borik asit ve sodyum tetraboratın S. aureus ATCC 25923, A. septicus DSM 19415, E. coli ATCC 35218 ve P. aeruginosa ATCC 27853 bakterilerine karşı bakterisid etkili olduğunu tespit etmiştir. Ayrıca Szałaj ve ark. 56, yaptıkları çalışmada lipopeptidaz ile esterifiye edilen boronik esterlerin E. coli type I signal peptidase (EcLepB) enzimini inhibe ederek E. coliye karşı iyi bir antibakteriyel etki gösterdiğini belirtmişlerdir. Yapılan başka bir çalışmada, heksagonal boron nitrit nanopartiküllerinin Streptococcus mutans 3.3, Staphylococcus pasteuri M3, Candida sp. M25 ve S. mutans ATTC 25175a karşı önemli antimikrobiyel etkiye sahip olduğunu, S. mutans 3.3, S. mutans ATTC 25175 ve Candida sp. M25 gelişimini engelleyerek ağızda biyofilm oluşumunu önlediği tespit edilmiştir 57.
7. Sonuç
Yapılan son çalışmalar, yeterli miktarda alınan borun sağlık üzerine olumlu etkisinin olduğunu ortaya koymaktadır. Ayrıca literatür bilgileri bor türevi moleküllerin bakteri, küf, maya ve virüslere karşı bakteriyostatik, bakterisidal, fungistatik, fungisidal ve antiviral etkilerinin olduğu ve bazı hastalıkların tedavisinde kullanılabileceğini göstermektedir. Bor, gıda takviyelerinde ve gıdalarda koruyucu olarak kullanılmakta ayrıca borun son zamanlarda gıda ambalaj malzemelerinde kullanılmasına yönelik çalışmalar yapılmaktadır. Her ne kadar bor üzerinde sayısız denemeler son on yılda gerçekleştirilmiş olsa da borun hem mekanizmasını aydınlatmak için hem de gıda hijyeninde, et ve süt ürünlerinde ve yumurtada kullanımına yönelik çalışmalar yapılmalıdır.