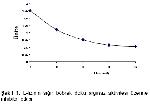
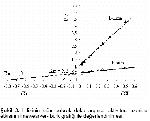
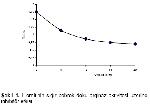
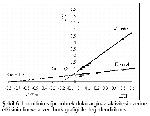
Bu çalışmada L-lizin ve L- ornitinin sığır böbrek doku arginazını karışık olarak inhibe ettiği, Km' lerinin inhibitörlü enzim kaynağında 5.2, inhibitörsüz enzim kaynağında (kontrol) ise 1.3 olduğu saptanmıştır. Bu amino asitlerin her ikisi de enzimin Vmax'ını kontrole göre düşürerek, Km' ini ise artırarak karışık inhibisyona (kompetetif-nonkompetetif) neden olmuştur. İnhibitör serbest enzime yada enzim-substrat kompleksine bağlandığı zaman inhibisyon karışık inhibisyon olarak adlandırılır. Bu inhibisyon tipinde inhibitör substratın bağlandığı aktif merkezden farklı bir yere bağlanır.
9.
Bu güne kadar farklı dokularda bu amino asitlerin inhibisyon etkisi çalışılmıştır. Amino asitler konusunda yapılan bu çalışmanın diğerlerinden farkı inhibitör etkisi olan bu amino asitlerin her ikisinin de sığır böbrek doku arginazını karışık olarak inhibe etmesidir.
Bond 10, nonkompetatif inhibisyona sebep olan inhibitörlerin substrattan farklı bir noktada enzimle reversible olarak birleştiği ve ligantların muhtemelen enzim substrat kompleksinin turnover' ını bozan konformasyonel değişime sebep olduğunu ve enzimin proteolitik inaktivasyona duyarlılığının arttığını belirtmiştir.
Rat beyin mitokondrisinde yaptıkları çalışmada 25 mM L-arginin kullanarak L- lizin ve L-ornitinin enzimi 20 kat inhibe ettiğini saptamışlardır 11.
Koyun meme doku arginaz aktivitesi 4 ve sığır sumen doku arginaz aktivitesi 3 üzerine L- lizin ve L- ornitin amino asitlerinin etkileri araştırılmış , her iki amino asidinde enzimi nonkompetetif inhibe ettiği tespit edilmiştir.
M. Expansa arginaz aktivitesi 12 , sıçan karaciğer arginaz aktivitesi 13, laktasyondaki rat meme bezi arginazı 14, Sığır karaciğer arginazı 15,16, İnsan tiroid doku arginaz aktivitesi 17, Xenopus laevis karaciğer arginazı 18, Mus booduga (Gray) karaciğer arginazı 19, üzerine L- Lizin ve L- ornitin amino asitlerinin inhibisyon etkisi incelenmiş ve bu amino asitlerin enzimi kompetetif inhibe ettikleri ortaya konmuştur..
İnsan karaciğer arginazını ornitinin nonkompetatif, lizinin ise kompetetif inhibe ettiğini ortaya koymuşlardır 20.L- ornitinin buzağı karaciğer arginazını 21, ve vitreus arginazı 22 üzerindeki etkisini incelenmiş ve bu amino asidin enzim üzerinde kompetetif inhibisyona neden olduğunu saptanmıştır.
Kaysen ve strecker böbrek dokusunda yüksek arginin konsantrasyonlarıyla enzimin aktivasyonunun, prolin ve lizin amino asitlerinin belirli konsantrasyonları ile engellenebildiğine işaret etmişlerdir 23. Koyun karaciğer dokusunda 55 mM' lık lizinin arginaz aktivitesini % 74 oranında inhibe ettiği ve inhibisyon tipinin karışık olduğu bulunmuştur 24. Ameen ve Palmer' de lizinin karaciğer arginazının karışık inhibisyonuna sebep olduğunu belirtmişlerdir 25.
Koyun beyin doku arginazı üzerine bazı L- amino asitlerin inhibisyon etkisi incelendiğinde lizin, ornitin, lösin ve valinin kompetetif inhibisyona neden olduğu tespit edilmiştir 26. Ornitin, lizin ve prolin koyun karaciğer arginazı üzerinde kompetetif inhibisyona neden olurken valinin Mn+2 ile aktive edilmemiş enzimde karışık tip inhibisyona sebep olduğu saptanmıştır 27.
Sığır rumen doku arginazı üzerinde valin, lösin, izölösin, prolin, sistein gibi bazı L- amino asitlerin nonkompetetif inhibisyona neden olduğu bildirilmiştir 28.
Sonuç olarak sığır böbrek doku arginazı üzerine L- Lizin ve L- Ornitin amino asitlerinin inhibisyon etkisi ilk defa laboratuarımızda çalışılmış olup her iki amino asidin de enzimi karışık tip inhibisyona uğrattığı tesbit edilmiştir. Amino asitlerden . L-Ornitin ile ilgili bulduğumuz sonuçlar literatürlerden farklı, .L-lizin ile ilgili bulduğumuz sonuçların ise Benzer 24 ile Ameen ve Palmer 25 tarafından yapılmış çalışmalarla uyum içerisinde olduğu gözlenmektedir.