Farklı doku ve organlardan köken alan hücrelerin metabolizma hızları, detoksifikasyon yetenekleri, oksidatif strese dayanıklılıkları ve yaşam süreleri birbirinden farklıdır. Bu nedenle farklı hücre hatlarında aynı kimyasal maddenin lethal dozları farklılık göstermektedir. Nakamura ve Liptan
15'ın nöroblastoma (SK-N-SH) hücreleri kullanarak paraquatın apoptotik etkilerinin araştırdıkları çalışmada, 200 µM konsantrasyonda paraquat, bu hücre hattında 18 saat inkubasyon için IC50 değeri olarak belirlenmiştir. 32D/Neo fare miyeloid hücre hattında paraquatın apoptotik etkilerinin incelendiği bir çalışmada ise 400 µM dozunda uygulanan paraquatın, 24 saatlik inkubasyon sonunda hücrelerin yaklaşık % 30'unu öldürdüğü bildirilmiştir
16. Cappelletti ve ark.
17'nın insan akciğer epitel hücre hattı olan A549 kullanarak paraquat toksisitesi ve antioksidanların bu toksisite üzerine koruyucu etkilerini inceledikleri çalışmada, 160 µM paraquat ile 24 saat inkubasyona bıraktıkları hücrelerde 24. saat sonunda apoptozisin indüklendiğini belirtmişlerdir. Paraquat'ın HepG2 hücre hattında IC
50 değerini belirlemek amacıyla hücre çoğalması ve canlılığının in vitro ortamda belirlemesinde bir kriter olan MTT testi uygulanmıştır. Hücrelerin 24 saat inkubasyon sonunda % 50 oranında öldüğü yani IC
50 konsantrasyonu olarak 10 µM belirlenmiştir. Çalışmada belirlenen 10 µM konsantrasyondaki paraquatın IC
50 dozu yukarıda belirtilen çalışmalarda bildirilen konsantrasyonlardan daha düşük dozda olduğu görülmektedir. Niso-Santano ve ark.
18'nın rat beyin nöroblast hücre hattında ( E18 ) yaptıkları çalışmada ise, düşük doz paraquatın (2.5 µM konsantrasyonda) 24 saat inkubasyon sonunda hücrelerin % 50'sini öldürdüğünü bildirmektedir
18.
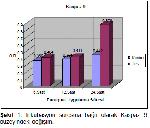
Çalışmada, paraquatın HepG2 hücreleri üzerine etkisini hangi metabolik yol üzerinden gösterdiğini anlayabilmek amacıyla, intrinsik apoptozis yolunda önemli rol oynayan kaspaz 9 enziminin aktivasyonu, paraquat inkubasyon süresine bağlı olarak incelenmiştir. Kaspaz 9, başlatıcı kaspazlar grubu içerisinde bulunan ve mitokondri aracılı apoptoziste rol alan aspartik asit spesifik proteazdır19. Prokaspaz 9'un aktive olabilmesi ve kaspaz kaskadını başlatabilmesi üç aşamada olur. İlk olarak dATP/ATP, APAF-1'e bağlanır ve hidroliz olarak ADP'ye dönüşür. İkinci aşamada sitokrom C APAF-1‘e bağlanır ve multimerize olur, son aşamada ise prokaspaz 9 bu multimerik yapıya bağlanır ve otokatalizasyonla aktive olur. Aktive olan kaspaz 9, APAF kompleksinden serbest hale geçer ve diğer kaspazları uyararak apoptozisin devamını sağlar20. Lopez ve Ferrer21, nöroblastoma hücrelerinde diğer apoptozis belirteçleri pozitif olmasına rağmen kaspaz 9'un aktive olmadığını, intrinsik olarak apoptozisin uyarılması durumunda kaspaz 9'un aktivasyonunun şart olmadığı, sitokrom C'nin kaspaz kaskadının başlatılmasında kilit rol oynadığını bildirmişlerdir. Xu ve ark.22, alisom B asetat kullanarak gastrik adenokarsinom hücre hattında yaptıkları çalışmada, doza bağımlı olarak apoptozis yüzdesinin yükseldiğini, kaspaz 9 ve kaspaz 3 ifadesinin arttığını ve buna paralel olarak pro-apoptotik protein olan Bax miktarındaki artış ile Bax/Bcl-2 oranının yükseldiğini bildirmişlerdir. Sonlandırıcı kaspaz olan kaspaz 3 aktivasyonu için kaspaz 9'un mutlaka aktive olması gerektiği ve sitokrom C'nin mitokondri dış membran potansiyelindeki azalma ile sitoplazmaya salıverilmesinin gerektiği sonucuna varmışlardır22. HepG2 hücrelerinin paraquat ile inkubasyon süresinin 6. saatinde kontrol ve deneme grupları arasında kaspaz 9 düzeylerinde istatistik olarak fark bulunmazken, 12. ve 24. saatlerde deneme gruplarında kaspaz 9 aktivasyonunun arttığı gözlenmiştir.
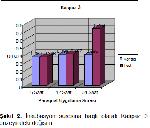
Efektör kaspazlar kendilerine spesifik proteinleri parçalayarak apoptotik hücre morfolojisinin meydana gelmesine neden olurlar23. Pro-kaspaz 9'un aktive olması sonucu kaspaz yolu aktive olur ve bunun sonucunda da efektör kaspaz olan kaspaz 3 aktivasyonu gerçekleşir24. Çalışmada, efektör kaspaz olan kaspaz 3 aktivasyonunun zamana bağlı olarak değişimine bakıldığında, inkubasyon süresinin 6. ve 12. saatlerinde kontrol ve deneme grupları arasında istatistiksel bir fark bulunmazken, 24. saatte kaspaz 3 aktivasyonunun arttığı ve gruplar arasındaki farkın istatistiksel olarak önemli olduğu görülmüştür.
Nöroblastoma hücrelerinde staurosporinin uyardığı apoptozis sırasında inkubasyonun 12. saatinde kaspaz 3 seviyesinin en üst düzeye çıktığı bildirilmiştir21. Median ve ark. (25)'nın flavanon türevi olan (3aRS,4SR)-2- (2 – chloro – 4 – methylsulfonylphenyl) – 4 – chloro - 3, 4-diethoxy-flavane[4,3- d]-D1,9b-1,2,3-thiadiazoline) MAFTZ'nin hepatosellüler karsinom hücreleri üzerinde apoptotik etkilerini araştırdıkları çalışmada, apoptotik etkinin doz ve zamana bağlı olarak kaspaz 3 aktivasyonu ve poly (ADP-riboz) polimeraz aktivasyonunun meydana geldiğini bildirmişlerdir. Buna ek olarak ROS miktarında artış ve mitokondrial membran potansiyelinde kayıp olduğu ve bunun sonucunda da ölüm sinyalinin mitokondrial oksijen stres yolağından kaynaklandığı gösterilmiştir.
Son yıllarda yapılan çalışmalarda bazı kanser hücre hatlarında kaspaz 3'ün belirlenebilir limitlerin çok altında sentezlendiği ortaya konulmuştur. MCF-7 hücre hattında yapılan bir çalışmada bunun nedeninin kaspaz 3 genindeki (CASP-3) parsiyal delesyondan kaynaklandığı ortaya konulmuştur26. Kanserin oluşum nedenlerinden biri apoptozisi kontrol eden genlerin mutasyonu ve sonucunda da kaspazların sentezinde azalma ya da hiç sentezlenememesidir. Olası kanser terapötik ajanlarının geliştirilmesi, bu enzimlerin sentezlerinin uyarılabilmesinin sağlanması esasına dayanır.
Primer hepatosellüler karsinom hücreleri ile Sun ve ark.27 tarafından yapılan çalışmada, in-situ hibridizasyon yöntemi ile kaspaz 3 gen ifadesi ölçülmüş ve kanserli dokularda normal karaciğer dokusuna oranla kaspaz 3 ifadesinin düşük olduğu ve ayrıca diferansiyasyon ve kaspaz 3 arasında ilişki olduğu bildirilmiştir. Kaspaz 3 ifadesindeki azalmanın HCC oluşumunda etkili olduğu sonucuna varılmıştır.
Çalışmada dikkat çeken bir nokta da kaspaz 9 ve kaspaz 3 aktivasyonlarının inkubasyon süresine göre farklılık göstermesidir. İnkubasyonun 12. saatinde ilk olarak başlatıcı kaspazlardan olan kaspaz 9 aktive olmuş bunu takiben kaspaz 3 inkubasyonun 24. saatinde aktive olarak apoptotik süreci devam ettirmiştir. Bu ard arda devam eden süreç bugüne kadar tanımlanmış kaspaz kaskadı fenomeni ile uyumludur.
Kaspaz 3'ün aktive olması ile sitoplazma ve nükleus içerisinde hedef proteinler yıkılır. Nükleus içerisindeki hedef proteinlerden biri de DNA endonükleaz ile çapraz bağlanma yapan bir proteindir (PARP). Kaspazlar bu proteini yıkarak endonükleazı aktifleştirir, endonükleazın aktifleşmesi ile 180 baz çifti ve katları şeklinde kırıklar oluşur ve DNA laddering paterni meydana gelir23. HepG2 hücrelerinde 10 µM dozunda paraquat inkubasyonunun 6., 12. ve 24. saatlerinde DNA üzerinde kırıklar oluşturup oluşturmadığını incelemek amacıyla çekirdek DNA'sını izole ettikten sonra agaroz jel elektroforez uygulaması gerçekleştirilmiştir. Kontrol ve deneme gruplarında 6., 12. ve 24. saatlerde belirgin bir DNA kırılması gözlenememiştir. DNA laddering testi, kitlesel hücre ölümlerini ve çok miktarda DNA'nın yıkımlanmasını gösterebilen bir testtir. 32D/Neo fare miyeloid hücre hattında paraquatın apoptotik etkilerinin incelendiği bir çalışmada16, 400 µM dozunda uygulama sonucunda DNA laddering görünümünün ortaya çıktığı bildirilmiştir. MCF-7 hücre hattında, çeşitli apoptozis uyarıcıları ile (TNF/sikloheksimid, staurosporin) yapılan çalışmalarda, hücre ölümünün DNA fragmentasyonu olmadan gerçekleştiği bildirilmiştir. Diğer yandan HeLa D98 hücrelerinde aynı uyarıcılar kullanıldığında, apoptozisin meydana geldiği fakat MCF-7 hattından farklı olarak bunlarda DNA fragmentasyonunun da oluştuğu görülmüştür26. Daha hassas ve tek hücre bazında sonuç verebilen TUNEL testinin ileride yapılacak çalışmalarda DNA laddering testi yerine kullanılması tavsiye edilmektedir28.
Paraquat dozuna bağlı olarak sitozolde sitokrom C miktarının arttığı ve bu artışın kaspaz aktivasyonundan bağımsız olarak meydana geldiği ortaya konulmuştur15. Sitokromlar elektron taşıyan proteinler olup, hemoglobinin hem halkasına benzer bir porfirin halkasına bağlı demir içerir. Sitokrom C, apoptozis sırasında kolayca sitoplazmaya geçebilen küçük bir moleküldür. Diğer sitokromlar ise mitokondri iç membranında yer alan proteinlerdir. HepG2 hücrelerinde, paraquatın sitokrom C düzeyi üzerine etkisini incelemek amacıyla inkubasyonun 6., 12. ve 24. saatlerinde hücre içi toplam sitokrom C miktarı ELISA yöntemi ile ölçüldü. Belirtilen saatlerde kontrol ve deneme grupları arasında sitokrom C düzeylerinde fark bulunamadı. İntrinsik hücre ölüm yolunda kilit rolü sitokrom C oynar. Nöroblastoma hücrelerinde paraquatın apoptozisi başlatması intrinsik hücre ölüm yolu üzerinden olduğu bildirilmiştir. Sitokrom C'nin sitozole salınımı ve kaspaz 3 aktivasyonu sonucu apoptotik hücre ölümleri şekillenmesine rağmen mitokondri membran geçirgenliğinde herhangi bir fonksiyon bozukluğu gözlenmemiştir29.
Sonuç olarak, HepG2 hücrelerinin 10 µM paraquat ile inkubasyonu sonucu Kaspaz 9 ve kaspaz 3 aktivasyonları inkubasyon süresine göre farklılık göstermektedir. İnkubasyonun 12. saatinde ilk olarak başlatıcı kaspazlardan olan kaspaz 9 aktive olmakta bunu takiben inkubasyonun 24. saatinde kaspaz 3 aktive olmaktadır. Bu ard arda devam eden aktivasyon ile bugüne kadar tanımlanmış kaspaz kaskadı fenomeniyle uyumlu olarak apoptotik süreç başlamıştır.
Son yıllarda üzerinde durulan konulardan birisi de kanser kemoterapisi sırasında antioksidanların verilmesi, antineoplastik etkinliği engeller mi yada kemoterapi sırasında oluşan yan etkilerin gelişimini önler mi olmaktadır. In vitro sistemlerde ve bazı hayvan deneylerinde elde edilen sonuçlar, kemoterapi sırasında antioksidatif dozda vitaminlerin kullanılmasının yararlı olduğunu gösterse de halen klinik çalışmalar devam etmektedir. Burada en önemli nokta kullanılan kemoterapötik ajanın oksidatif stres yaratarak apoptozis yoluyla öldürmeye çalıştığı kanser hücrelerini, dışarıdan verilen antioksidanlarla apoptozise gitmesini engellememelidir. Bununla beraber, eğer kemoterapötik uygulaması ile oluşan radikaller ilacın sadece yan etkilerinden sorumlu yani ilacın antineoplastik aktivitesinden sorumlu değilse, antioksidanların kullanımı ilacın yan etkilerinin en aza indirilmesi için yararlı olabilir. Bu nedenle oksidatif stres oluşturulan hücrelerde antioksidanların etkilerinin incelendiği çalışmalara yer verilmelidir.
Teşekkür
Çalışmada kullanılan HepG2 hücre hattı Gazi Üniversitesi Tıp Fakültesi İmmunoloji Anabilim Dalı Başkanı Prof. Dr.Cemalettin Aybay'dan temin edilmiştir.