Araştırma ve Yayın Etiği: Çalışmaya Hayvan Deneyleri Yerel Etik Kurulu Başkanlığının resmi onayı alındıktan sonra başlanmıştır (20.04.2016, Karar no: 82).
Grupların Oluşturulması: Materyal olarak Fırat Üniversitesi Deneysel Araştırma Merkezinden elde edilen 30 adet dişi, erişkin, 250-300 ağırlığındaki Wistar Albino rat kullanıldı. Ratlara özel kafesler içerisinde, özel laboratuvar koşulları uygulanarak bakıldı (24±3℃ %40-60 nem, 12 saat karanlık 12 saat aydınlık). Beslenmesi standart pelet yem kullanılarak yapıldı. Çalışma için ratlar rastgele üç gruba ayrıldı. Birinci gruptaki ratların sağ gözlerinde alkali yanık oluşturulduktan sonra 20 gün sığır amniyon sıvısı damlatıldı (AS). İkinci gruptaki ratların sağ gözlerinde alkali yanık oluşturulduktan sonra 20 gün serum fizyolojik damlatıldı (PK). Üçüncü gruptaki ratlara herhangi bir işlem uygulanmadan 20 gün boyunca sığır amniyotik sıvısı uygulandı (NK).
Anestezi Protokolü: Korneada alkali yanık oluşturulması için, ratlar genel anesteziye alındı. Bu amaçla intramusküler yolla 4 mg/kg xylazine hidroklorür (Rompun®; 23.32mg/mL, Bayer, İstanbul, Türkiye) ve yine intramusküler yolla 50 mg/kg ketamin hidroklorür (Ketalar®; 50 mg/mL, Eczacıbaşı, İstanbul, Türkiye) uygulandı.
Korneada Alkali Yanık Oluşturulması: Anesteziye alınan ratlara, korneda alkali yanık oluşturulmadan önce %0.5 lik proparakain HCI (Alcain %0.5, Alcon, Istanbul, Turkey) uygulanarak lokal anestezi sağlandı. AS ve PK gruplarındaki ratların sağ gözlerinde alkali kornea yanığı oluşturuldu. Bunun için 3 mm çapında bir filtre kağıdına 2N yoğunluğundaki NaOH emdirilerek 40 saniye kornea üzerinde bekletildi. Alkali yanık oluşturulduktan sonra AS ve PK grubundaki ratların sağ gözleri serum fizyolojik ile 2 dk boyunca yıkandı. NK grubundaki ratların gözlerinde alkali yanık oluşturulmadı.
Amniyon Sıvısının Hazırlanması: Çalışmada sağlıklı gebe ineklerden sezeryan operasyonu sırasında elde edilen amnion sıvısı kullanıldı. Operasyondan hemen sonra steril şartlarda toplanan amniyon sıvısının laboratuarda bakteriyolojik muayeneleri yapıldı. Sağlıklı oldukları anlaşılan amniyon sıvıları 2000 devirde 15 dakika süreyle santrüfüj edildi. Santrüfüj işlemi sonunda supernatant olarak ifade edilen kısım alınarak steril tüplere yerleştirildi ve denature olmaması için dondurularak -20 ⁰C sıcaklıkta saklandı. Kullanıma başlamadan 1 gün once +4 ⁰C de bekletilen amniyon sıvısı göze damlatma şeklinde kullanıldı 33.
Amniyon Sıvısının Kullanımı: AS ve NK gruplarındaki ratların sağ gözlerine 20 gün boyunca, günde üç kez 2şer damla sığır amniyon sıvısı damlatıldı. PK grubundaki ratların ise sağ gözlerine 20 gün boyunca, günde üç kez 2şer damla serum fizyolojik damlatıldı.
Klinik Bulguların Tespiti: Bütün gruplardaki ratlara 1, 5, 10, 15 ve 20. günlerde Schirmer testi, rose bengal boyama, fluorescein boyama, gözyaşı kırılma zamanı tayini ve göz içi basınç ölçümü yapıldı.
Çalışma süresince ratlarda görülmesi muhtemel fotofobi, blefarospazm, konjunktivitis, korneal hasarlar (korneal vaskülarizasyon, ödem, perforasyon vs.) gibi oküler değişikliklerin takibi ise oftalmoskop (Heine Omega®500 Indirect Binocular Ofthalmoskop, Almanya) ile yapıldı.
Schirmer Testi: Bu amaçla Zone-Quick (Shoma Yakuhın Kako Co Ltd. Tokyo/Japonya) marka bir gözyaşı ölçüm ipliği kullanıldı. Bunun için her bir rat uzman kişilerce dikkatli bir şekilde tutularak iplikçik sağ alt göz kapağının konjunktival boşluğuna yerleştirildi. Bir dakika sonra alınarak gözyaşı miktarı kendi ölçüm çubuğunda değerlendirildi.
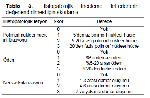
Rose-Bengal Boyama: Bu testte ratların sağ gözlerine bir mikro enjektör (901 N, Hamilton, Amerika Birleşik Devletleri) ile %1lik Rose bengal (Institut Pourquier, Monpellier Fransa) boyasından 1 μl damlatıldı. Uygulamadan 5 dakika sonra boyanmış olan kornealar endirekt oftalmoskop ile 20 dioptrilik bir lup kullanılarak beyaz ışık altında muayene edildi. Bu parametre ile korneada saptanan değişimler Tablo 1de gösterildiği şekilde derecelendirildi 8,19.
Fluorescein Boyama: Bu testte ratların sağ gözlerine bir mikro enjektör (901 N, Hamilton, ABD) ile %1 lik sodyum fluorescein (Bereket Kimya Lab. İstanbul, Türkiye) boyasından 1 μL damlatıldı. Uygulamadan 5 dakika sonra boyanmış olan kornealar endirekt oftalmoskop ile 20 dioptrilik bir lup kullanılarak kobalt mavisi filtresi altında muayene edildi. Bu parametre ile korneada saptanan değişimler Tablo 2de gösterildiği şekilde derecelendirildi 8,19.
Gözyaşı Kırılma Zamanı: Ratların sağ gözlerine %1lik sodyum fluorescein solüsyonundan 1 μL damlatıldıktan sonra tam bir göz kırpma gerçekleşmesi beklendi. Daha sonra endirekt oftalmoskop ile 20 dioptrilik bir lup kullanılarak beyaz ışık altında dikkatli bir şekilde incelenerek ikinci bir göz kırpmasına müsaade edilmeksizin korneadaki kırılmanın ilk göstergesi olan ilk siyah kuru nokta görülmesine kadar geçen süre kaydedildi 8,19.
Göz içi Basıncın Ölçülmesi: Ratlar anesteziye alınmadan bir yardımcıya tutturularak Reıchert Technologies Tono-Pen marka bir tonometre tüm gruplarda göz içi basınç ölçümü yapıldı.
Ötenazi Protokolü: Histopatolojik verilerin elde edilmesi için 20. günün sonunda hayvanlar kapalı kutu içerisinde karbondioksit inhalasyonu ile ötenazi edildi. Ötenazi işleminden sonra histopatolojik değerlendirmeler için ratların sağ gözlerinden örnekler kullanıldı.
Histopatolojik Değerlendirmeler: Alınan korneal doku örnekleri %10luk nötral tamponlu formalinde tespit edildi. Rutin alkol ksilol serilerinden geçirilen örnekler parafin bloklara alındı. Bloklardan 5 μ kalınlığında alınan kesitler Hematoksilen-Eozin ile boyanarak ışık mikroskobunda incelendi. Histopatolojik incelemelerde ödem, neovaskülarizasyon ve polimorf nükleer hücre infiltrasyonlarının varlığı yönünden değerlendirmeler Tablo 3deki gibi yapıldı.
İstatistiksel Analiz: Klinik bulguların istatistiksel analizlerinde SPSS Ms Windows Release 16.0 programı kullanılmıştır. Veriler ortalama ± SD olarak ifade edilmiştir. Grup ortalamaları arasındaki farklar tek yönlü varyans analizi (ANOVA) kullanılarak tahmin edilmiş ve çoklu karşılaştırmalar Duncan testi kullanılmıştır. Histopatolojik incelemede semikantitatif olarak elde edilen verilerin gruplar arası farklılığı Kruskal Wallis testi, farklılığı oluşturan grupların tespiti Mann Whitney U testi ile belirlendi. P<0.05 değeri istatistiksel açıdan anlamlı olarak kabul edilmiştir 42.