Koronavirüsler (CoV'ler), pozitif anlamda, tek sarmallı genomik RNA'ya sahip zarflı virüslerdir ve dört cinse ayrılır: α-CoV'ler, β-CoV'ler, γ-CoV'ler ve δ-CoV'ler
1. Memelileri etkileyenler α- ve β-CoV'ler iken, diğer iki cins ise kuşları ve memelileri enfekte etmektedirler
2. Çin Halk Cumhuriyeti'nin Wuhan kentinde, Aralık 2019'da nedeni bilinmeyen bir dizi pnömoni hastasından koronavirüsün teşhis edilmesi son zamanlarda ortaya çıkan küresel salgın bakımından endişe vericidir. Salgın, canlı egzotik hayvanların satışının yapıldığı Wuhan Toptan Deniz Ürünleri Pazarı'ndaki işçilerle ilişkilendirilmiştir
3. Hastalık etkeni, 2002-2003 yılları arasında görülen ve şiddetli akut solunum sendromu (SARS) salgınından sorumlu olan SARS-CoV-1'e benzerliği (genomik olarak % 70) göz önüne alındığında SARS-CoV-2 olarak adlandırılmıştır. Bu yeni koronavirüs türünün resmi ve kabul edilen adı, koronavirüs bulaşıcı hastalık 2019'un kısaltması olan Covid-19 virüsüdür
1.
Günümüzde, Covid-19 için spesifik bir tedavi yoktur. En umut verici olarak önceden bilinen hidroksiklorokin ve Remdesivir ilaçlarının etkinliğini belirlemede klinik çalışmalar yapılmıştır 4. Ayrıca, SARS-CoV-2 enfeksiyonu geçirmiş ve iyileşen bireylerden alınan plazma (nötralize edici antikorlar içeren) kullanılarak yapılan transfüzyon çalışmaları sonucunda olumlu bulguların elde edildiği bildirilmiştir 5.
Bununla birlikte aşılama, bulaşıcı hastalıkların kontrol edilmesi ve ortadan kaldırılması için en etkili yaklaşım olmaktadır. Aşılar, konakçının hastalığa yakalanmadan önce, etkene karşı bağışıklık oluşmasını sağlayan biyolojik maddelerdir. Hastalığa neden olan patojen etkenin zayıflatılmış veya inaktif hale getirilmiş şekillerini ya da patojenin, bağışıklık sistemi tarafından tanınmasını sağlayan proteinleri içermektedirler. SARS-CoV-2 yüksek bulaşıcılığa sahip olduğundan bu etkene karşı mücadelede aşıların geliştirilmesi acil bir hedeftir. Aşı üretmenin basit yolu, daha önce kimyasal veya fiziksel olarak etkisiz hale getirilmiş SARS-CoV-2 viryonları ile formüle edilebilen etkisizleştirilmiş aşı teknolojisidir. Canlı zayıflatılmış virüs temelli aşı üretimi bir diğer olası yaklaşımdır 6. SARS-CoV-1 ve MERS-CoV için inaktif edilmiş aşı adaylarında, virüs nötralizasyonuna yol açan güçlü hümoral tepkiler ortaya çıkmıştır. Örneğin, influenza virüsü, SARS-CoV-2 antijenlerini açığa çıkarmak ve solunum yolu hastalıklarına neden olan ilgili etkeni hedef alan bivalan aşının oluşturulmasında yapısal iskelet olarak kullanılmaktadır 7. Benzer şekilde, adenoviral vektörler de bu alanda uygulanabilmektedir 8. Virüslere karşı geliştirilen tüm aşılar, güvenirliklerinin yanı sıra viral enfeksiyonun antikora bağlı olarak artması, reaktojenite ve suşun patojenik formlara dönüşmesi ile ilgili endişelerleri de beraberinde getirmektedir 9.
CoV'ların konak hücreye girişi, CoV spike proteinlerinin reseptör tanıma ve membran füzyon fonksiyonları aracılığıyla gerçekleşmektedir. Aşının birincil amacı CoV spike proteinlerini nötralize eden antikorlar oluşturmaktır. Sitotoksik T-lenfosit (CTL) yanıtları da viral enfeksiyonlara karşı korumada anahtar rol oynamaktadır 10. Bu ilkeler çerçevesinde, Covid-19'a karşı aşı geliştirme çalışmaları başlatılmıştır. Yapılan çalışmalar arasında CureVac 11,12 tarafından tam uzunlukta, prefüzyonla stabilize edilmiş bir Sproteinini kodlayan mRNA'yı taşıyan lipid nanopartikül (LNP: Lipid nonoparticle) ile formüle edilmiş RNA bazlı aşıların geliştirilmesi yer almaktadır 13. Shenzhen Geno-Immune Medical Institute tarafından geliştirilen diğer bir aşı adayı da viral antijenleri eksprese etmenin bir yolu olarak transdüksiyon yoluyla yapay antijen hücrelerinin üretilmesi ve sonuç olarak da T hücrelerinin aktive edilmesi amacıyla bağışıklık modülatör gen temeline dayanan multiepitopik bir aşıdan oluşmaktadır 14. Covid-19a karşı aşı geliştirilmesinde SARS-CoV-1 virüsü ile benzerlikler, değerli bir referans teşkil etmektedir. Ancak ikiden fazla varyant tanımlandığı için SARS-CoV-1'in genetik değişkenliğinin daha yüksek olduğu göz önünde bulundurulmalıdır. Bazı SARS-CoV-1'in nötralize edici antikorlarının, SARS-CoV-2 ile çapraz reaksiyona girmesi konusunda kapsamlı araştırmalara ihtiyaç vardır. SARS-CoV-1 ve SARS-CoV-2 arasında tanımlanan epitoplar aşı geliştirme için önerilmiştir 15.
Covid-19 hakkındaki temel bilgiler, aşı tasarımının iyileştirilmesi çalışmalarında faydalı olmaktadır. Örneğin, Walls ve ark. 16, aşıların ve viral giriş blokerlerinin tasarımında kritik öneme sahip olacak ektodomain trimerinin kriyo-EM yapılarını bildirmişlerdir. Ayrıca, SARS-CoV-1'e karşı murin poliklonal antikorları kullanarak SARS-CoV-2'nin konak hücrelere girişinin güçlü şekilde inhibe edildiğine dair kanıtlar da bulunmuştur. Bu virüsler arasında korunmuş S epitoplarının bağışıklama için uygun olabileceği ve belki de önceden var olan bağışıklama modellerinin Covid-19 ile mücadelede faydalı olacağı değerlendirilmektedir. Aşı tasarımındaki bu gelişmelere paralel olarak hızlı ve büyük ölçekli üretime uygun aşı platformlarının tanımlanması gerekmektedir. Özellikle de gelişmekte olan ülkelerde geniş kapsamlı aşılama kampanyaların uygulanmasında güvenli, düşük maliyet, kolay dağıtım ve teslimat olması gereken nitelikler arasında yer almaktadır. Aşılar çoğunlukla enjeksiyonla insan ve hayvanlara verilse de ağız ya da burundan sprey şeklinde uygulanan aşılar da bulunmaktadır. İnaktif veya zayıflatılmış özellikteki aşıların maliyetli olması, uygulama sırasında ve soğuk muhafaza koşullarında karşılaşılan zorluklar, insanların tamamına ulaşımının gerçekleşmemesi gibi çeşitli dezavantajları vardır. Bu nedenle 1990lı yılların başında genetik alanda yapılan çalışmalardan biri olan transgenik gen teknolojisi ile bitkilerden daha ucuz maliyetli, her kesimden insana kolay ulaştırılabilen ve ısıya dayanıklı yenilebilir aşı formu geliştirilmiştir 17.
Bitki Bazlı Yenilebilir Aşılar
Son dönemlerde bitkiler, ekzojen proteinlerin uygun şekilde çoğalmasını kolaylaştıran ve ekonomik olarak uygulanan yeni biyofarmasötik sistemlerin tasarlanmasında yaygın olarak kullanılmaktadır 18,19.
Geleneksel aşıların dezavantajlarına karşı son zamanlarda yenilebilir ürünlerin geliştirilmesi alanında araştırmalar yapılmıştır. Yenilebilir aşı üretiminde bitkilerin kullanılmasının çeşitli faydaları görülmüştür. Bunlardan ilki, biyofarmasötik endüstrisinde bitki aşıları daha düşük üretim maliyetlerine ve ölçeklendirilmeye sahiptirler 20,21. Bununla birlikte, biyomolekül üretiminden farklı olarak yenilebilir aşı formülasyonları uygulama öncesi herhangi bir tedavi veya saflaştırma gerektirmediğinden üretim maliyetinin düşmesine neden olmaktadır. Bu konuda yapılan araştırmaların çoğunda kültür patatesi kullanılmıştır. Ancak pişirme veya kaynatma işlemi antijenik proteinlerin çoğunun etkisinin zayıflamasına neden olabileceğinden, yenilebilir aşı üretiminde patates kullanımının iyi bir tercih olmadığı belirtilmiştir 22. Buna karşın, başarılı genetik dönüşüm yöntemlerinin tasarımı ve geliştirilmesi ile domates, mısır, tütün, muz, havuç ve yer fıstığı gibi bitkiler yenilebilir aşı üretiminde önem kazanmışlardır. Bugüne kadar, marul, domates, patates, papaya, havuç, kinoa ve tütün gibi yenilebilir çok sayıda bitki türü aşı antijenlerine dönüştürülmüştür 23.
Son zamanlarda, domuz gribi, kuduz ve hepatit B'ye karşı bazı bitkisel kökenli aşılarda klinik araştırmalar yapılmıştır. Bu araştırmalarda en umut verici sonuçlar influenza aşılarında tespit edilmiştir 24,25. Bu aşıların, insan ve fare hücrelerinde yapılan in-vitro testler sonucunda güvenilir ve bağışıklık oluşturma özelliklerinin pozitif olduğu değerlendirilmiştir 26.
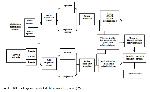
Bununla birlikte, düşük maliyetli aşı geliştirmenin nihai hedefinin saflaştırma gerektirmeden ve jelatin hapları veya tabletleri içinde dondurularak kurutulmuş özellikte oral formülasyonların üretilmesi olduğu belirtilmiştir 27. Bu oral aşılar, enjekte edilebilir aşıların uygulamasında ortaya çıkan ağrı gibi dezavantajların ve invaziv dağılım yolu ile ilişkili risklerin önlenmesinde de etkili olabilmektedir 28. Başlangıçta, beklenenden daha yavaş olduğu kabul edilmekle birlikte bitki bazlı oral aşıların geliştirilmesi bir gerçeklik kazanmıştır 27,29. Bitki bazlı aşıların geliştirilmesinde uygulanan olası yöntemler Şekil 1de gösterilmiştir 17.
Yenilebilir Aşıların Üretim Yöntemleri
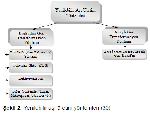
Yenilebilir aşılar, seçilen bitki hücresine transgenin dahil edilmesiyle üretilmektedir. Transgenin entegrasyonu, vektörle doğrudan veya dolaylı gen transferi yöntemiyle birleştirilmeden yapılabilmektedir. Yenilebilir aşı üretim yöntemleri Şekil 2de gösterilmiştir. Transgen, antijenin hücrelerle birleşmesi gereken yere bağlı kararlı transformasyon ve geçici transformasyon olmak üzere iki sistem ile bitkilerde eksprese edilebilmektedir 30.
Doğrudan Gen Transformasyon Yöntemi: Doğrudan gen transformasyonu basit bir yöntemdir. Bu yöntemde seçilen DNA veya RNA doğrudan bitki hücresine verilir. En yaygın kullanılan doğrudan gen transferi yöntemi biyolistik yöntemdir. Gen tabancası veya mikro mermi bombardımanı yöntemi olarak da bilinmektedir. Agrobacterium türlerinin aracılık ettiği gen transferinin mümkün olmadığı durumlarda kullanılmaktadır 31,32. Bu transformasyon yönteminde DNA veya RNA, mikro taşıyıcı görevi gören altın veya tungsten ile kaplanır. Daha sonra kaplanmış DNA gen tabancasına yerleştirilir ve yüksek basınç altında Helyum gazına maruz bırakılmaktadır. Kaplanmış DNA, yüksek basınç etkisiyle hareket ederek hedeflenen bitki hücresine yerleşmektedir. Ancak bu yöntem yüksek maliyetlidir 33,34. Nükleer transformasyon ve kloroplast transformasyon, biyolistik yöntemle yapılabilmektedir. Bunlar, iki tip antijen ekspresyon yöntemidir 35. Homolog olmayan genin rekombinasyon yoluyla bitki hücresinin çekirdeğine dahil edilmesi nükleer transformasyon olarak tanımlanmaktadır. Protein ekspresyonunu arttırmak için genin kloroplasta enjekte edilmesine ise kloroplast transformasyonu adı verilmektedir. Yenilebilir aşı üretiminde en yaygın kullanılan yöntem kloroplast transformasyonudur 36,37. Biyolistik yöntemler ile; kolera, Lyme hastalığı, şarbon, tetanoz, veba, rota virüsü ve köpek parvovirüsüne karşı aşı üretilmektedir 38.
Dolaylı Gen Transformasyon Yöntemi: Bu yöntemde vektör aracılığı ile bir gen transferi söz konusudur. Yöntemde, istenen bitki hücrelerine ilgili proteinin üretilmesi için bakteriler veya viral etkenler bulaştırılmaktadır 39.
Yenilebilir Aşı Modeli Olarak Kullanılan Başlıca Bitki Türleri
Patates: Bu ürün, tetanoz, difteri, hepatit B ve Norwalk virüsüne karşı yenilebilir aşı üretiminde uygun bir numunedir. Escherichia coli suşlarının neden olduğu enterite karşı patatesten yenilebilir aşı geliştirilmesine yönelik ilk denemeler yapılmıştır 40. Ayrıca, vizon enterit virüsüne karşı patatesten yenilebilir bir aşı da geliştirilmiştir. Patatesten yenilebilir aşı üretmenin temel faydası, dönüştürme ve çoğaltma kolaylığına sahip olmasıdır. Depolama için buzdolabına ihtiyaç yoktur. Başlıca dezavantajlardan biri pişirilmesi antijenlerin denatüre olmasına yol açmaktadır 41.
Pirinç: Yenilebilir aşıların geliştirilmesinde kullanılan bir diğer bitki türüdür. Pirinç, diğer bitkilere göre bebek mamasında ve yüksek antijen ekspresyonunda yaygın olarak kullanılmıştır. Ancak yavaş büyür ve sera koşuluna ihtiyaç duyulmaktadır. 2007 yılında, Oryza sativa adlı transgenik pirinçte yapılan bir araştırmada E. coli'ye karşı önemli miktarda antikor oluşmuştur. HBsAg'nin pirinç tohumlarındaki fonksiyonel ifadesi 2008'de onaylanmıştır. Pirinç bitkisinden geliştirilen aşıların halk sağlığı üzerinde etkili olacağı belirtilmektedir 41,42.
Muz: Yaygın olarak yenilebilir aşı üretiminde kullanılan bitki türüdür. Pişirmeye ihtiyaç duymamaktadır. Pişirildikten sonra proteinlerin yok edilmediği belirtilmiştir. Yaprakları antijen içermektedir. Başlıca dezavantajı, meyve vermesinin 2-3 yıl sürmesi ve meyvesinin olgunlaştıktan sonra hızla bozulmasıdır 43.
Domates: Koronavirüsün neden olduğu akut solunum yolu sendromu (SARS)' na karşı etkili ilk aşı, domates kullanılarak yapılmıştır. Norwalk virüsüne karşı patatesten üretilen aşılardan daha iyi etki göstermektedir. Domatesin yaprakları, gövde, meyve ve diğer dokuları Vibrio cholera B toksininden CT-B proteinlerini eksprese etme yeteneğine sahiptir 44. Ayrıca HBsAg'yi eksprese etmek için de domatesler kullanılmıştır. Bu bitkiden beta-amiloid proteinlerinin ekspresyonu ile Alzheimer hastalığına karşı etkili bir aşı geliştirilmiştir. Ayrıca domatesten pnömoni, septisemi ve bubonik (hıyarcıklı) veba aşılarının da geliştirildiği bildirilmiştir. Hızlı büyüme ve geniş çapta yetiştirilebilme özelliğine sahip bitkidir. Domates, bileşiminde yer alan yüksek A vitamini ile bağışıklık tepkisini artırabilmektedir. Ancak, çabuk bozulabilme özelliğine sahip bitkilerdir 44,45.
Marul: Bu bitki hem hayvanlar hem de insanlarda E. coli'nin neden olduğu enterik hastalıklara karşı etkili olan model bir bitkidir. Evcil ve yaban domuzların en bulaşıcı viral hastalıkları arasında yer alan Domuz virüsü olarak da bilinen Klasik Domuz Veba Virüsü (Classical Swine Fever Virus)ne karşı glikoprotein E2 eksprese edilmiş marul geliştirilmiştir. Bu bitki başlıca taze olarak tüketilir ve hepatit B virüsüne karşı faydalı etkilere neden olmaktadır. Yenilebilir aşı olarak kullanılabilecek son derece etkili bitkidir 46.
Tütün: Yenilebilir bir bitki olmamasına rağmen yenilebilir aşıların geliştirilmesinde örnek olarak kullanılmaktadır. Gastroenterite neden olan Norwalk virüsü için 1996 yılında tütünden bir aşı geliştirilmiştir. Transgenik tütün, tavuk bulaşıcı anemisine karşı VP1 proteinini eksprese etme yeteneğine sahiptir. Ayrıca tütün, hepatit B ile ilgili bir polipeptidi eksprese etmektedir. Koksidiyoza karşı aşı geliştirilmesinde de kullanılmaktadır 47.
Havuç: Sadece sağlığa yararlı ve lezzetli değil, aynı zamanda yenilebilir aşı formları olarak da kullanılabilen bir bitkidir. HIV, E coli, Helicobacter pylori'ye karşı aşılar, transgenik havuçlarda üretildiğinde potansiyel etkileri görülmektedir. Bağışıklık sistemi zayıf olan kişilerde, bu tip antijen içeren yenilebilir havuç aşısının fayda sağlamayacağı belirtilmektedir 48.
Covid-19a Karşı Bitki Bazlı Aşı Geliştirme İmkanları
Geleneksel aşılara göre yenilebilir aşı geliştirilmesi yönteminin avantajları olmasına rağmen COVID-19a neden olan SARS-CoV-2ye karşı alternatif yenilebilir aşı üretim yöntemi çok az araştırılmıştır. Son yıllarda COVİD-19 sorunun çözümü amacıyla aşı niteliğindeki virüs proteinlerinin domateslerde üretilmesine odaklanılmıştır. Nitekim biyoinformatik yöntemler kullanılarak bağışıklık tepkisinin oluşması için en uygun aşı adayı olan antijenler tespit edilmektedir. Bu işlem, patojen etkenin genom yapısının bilgisayarda analizi ile gerçekleşmektedir. Daha sonra domatesin nükleotit dizilimi ve Agrobacterium tumefaciens bakterisi tarafından gerçekleştirilen transformasyonu en uygun hale getirilmektedir. Domates bitkilerinden yeni epitopların ekspresyonu sonucunda çok sayıda rekombinant proteini elde edilmektedir. SARSa neden olan SARS-CoV-1, COVID-19a sebep olan SARS-CoV-2 virüsü ile % 70 genomik benzerlik göstermektedir. Ancak geliştirilen transgenik domatesin deneysel olarak farelere verilerek SARS-CoV-1e karşı yüksek değerlerde antijen üretiminin kaydedildiği klinik çalışmalara devam edilmemiştir. Günümüzde SARS-CoV-1 virüsü ile olan benzerlik durumu rehber alınarak SARS-CoV-2nin genomik ve proteomik dizilimi kullanılarak bağışıklık cevabını oluşturacak en iyi antijenlerin elde edilmesi için biyoinformatik yöntemlerden yararlanılan analiz yapma süreci devam etmektedir 17.
Virüs Benzeri Parçacıklar (VLP'ler): Aşı tasarımı için öne çıkan bir yaklaşım, virüslere benzeyen, ancak genomları olmayan makromoleküler kompleksler olan virüs benzeri parçacıkların (VLP'ler) kullanımı temeline dayanmaktadır. Bu yöntemde, VLP'ler virüslerin doğal yapısına benzer ancak onlar kadar enfektif değildirler. Atenüe veya inaktif virüslerle formüle edilen, reaktojenite ve patojenik formlara dönüşen aşıların dezavantajları önlenmektedir 49. İnfluenza virüsü, insan papilloma virüsü, insan immün yetmezlik virüsü, şap hastalığı virüsü, Norwalk virüsü, rift vadisi ateşi virüsü ve hepatit B virüsünün neden olduğu vakalara karşı VLP'lerin üretimi konusunda çok sayıda araştırma bulunmaktadır 50,51.
VLP'lerin oluşumuna yol açan rekombinant sistemlerde ifade edilen SARS-CoV-1 ve MERS antijenlerin benzerleri Covid-19 aşısının geliştirilmesi yönünde önemli rehber oluşturmaktadır. Mortola ve Roy (2004) tarafından SARS- Cov için S (Spike), E (Zarf), M (Membran) ve N (Nükleokapsid) yapısal proteinlerini esas alan bakulovirüs/böcek hücreleri ekspresyonu (Sf 9 hücreleri) uygulayan koronavirüs VLP'leri üretilmiştir 52. 2007 yılında, ilk kez SARS-CoV-1 VLP'lerin immünojenitesi, M, E ve S proteinlerine dayalı böcek hücresi yapımı VLP'ler değerlendirilerek tanımlanmıştır. Enfekte böcek hücrelerindeki VLP oluşumu elektron mikroskop ile gözlemlenmiştir. Freund adjuvanı ile emülsiyon haline getirilen dört deri altı VLPnin kullanıldığı aşılama programına alınan farelerde SARS CoVa karşı yüksek antikor titreleri tespit edilmiştir 53.
Zarflı virüslerin VLP'lerinin bitkilerde Hemaglutinin (HA) proteinini başarılı bir şekilde eksprese etmesi dikkate alındığında, S proteinini de eksprese ederek SARS-CoV-2 VLP'lerinin birleştirilmesi mümkün olabilmektedir 54. Bu amaçla, VLP'lerin glikosilasyon ve salgılama mekanızması ile üretimin yapılması maksadıyla trans-Golgi salgılanmasını hedefleyen nükleer ekspresyonun bir proteine ihtiyacı olduğu bildirilmiştir 55. Bu nedenle, COVID-19a karşı bitki bazlı aşıların geliştirilmesi sürecinde bu çalışmaların kabul edilmesi faydalı olmaktadır. SARS-CoV-2 virüsüne benzeyen VLP'lerin yanı sıra, olası diğer bir yaklaşım SARS-CoV-2 epitoplarını kabul ederek kimerik VLP'lerde tanımlamaktatır. Bu durumda ilişkili olmayan bir virüsten alınan VLP, mevcut hedef SARS-CoV-2 epitoplarının yapısal iskeleti olarak görev yapabilmektedir 56.
Multiepitopik Aşılar: Koruyucu bağışıklık tepkilerini indükleyen epitoplar seçilerek sağlam ve potansiyel bir rasyonel aşı modeline sahip özellikte multiepitopik aşılar geliştirilmiştir. Özellikle rasyonel aşı tasarımında sadece immün koruma yönünden değil, aynı zamanda güvenliği bakımından da tekrarlama çalışmaları oldukça önemli olmaktadır 57.
Viral hastalığa karşı multiepitopik aşıların geliştirilmesinde önemli faktör, genetik değişkenliktir. Hatta, SARS-CoV 2 virüsünün iki ana tipi olan L ve S'ye dönüştüğü ileri sürülmüştür. L tipi (∼%70), S tipine (∼%30) karşı baskın ve S tipinden daha agresiftir. Tang ve ark. 58, salgın ortaya çıktıktan hemen sonra insana bulaşmasının engellenmesi ile L ve S tiplerinin prevalansının etkilendiğini bildirmişlerdir 59.
İmmun Kompleksleri: Bitkilerde immun komplekslerin (İK'ler) üretimi, yüksek oranda immünojenik ajanlar oluşturan başka bir yaklaşımdır. İK'ler, antijen sunan hücreler tarafından verimli bir şekilde yakalanan ve işlenen makromoleküler varlıkları oluşturan, onları tanıyan antikorlarla kompleks haline getirilmiş antijenlerden oluşmaktadır 60. Protein sentezi ve işlenmesi için bitki hücrelerinden yararlanarak, antikor ve İK fabrikaları olarak kullanılmışlardır 61. Örneğin, bir monoklonal antikora kaynaştırılan tetanoz toksini fragmanı C'ye dayalı İK'ler, transgenik tütün bitkilerinde üretilmiştir 62. Bu yaklaşımın başlıca dezavantajı, henüz SARS-CoV-2 için mevcut olmayan antijeni hedefleyen tanımlanmış antikorlara olan ihtiyaçtır. Bununla birlikte, anti-SARS-CoV-1 S protein antikorlarının SARS-CoV-2 karşılık çapraz reaktivitesi rapor edilmiştir 3.
Elastin Benzeri Polipeptit Füzyonlar: Enjekte edilebilir aşıların üretiminin bir parçası olarak antijenlerin saflaştırılması zahmetli ve pahalı bir faaliyettir. Saflaştırma işlemini basitleştirmek için kullanılan alternatif yaklaşım, sıcaklığın değiştirilerek proteinin çökeltürülmesine izin veren, tersine çevrilebilir faz geçişi adı verilen benzersiz bir özelliğe sahip olan elastin benzeri polipeptitlerin (ELP) füzyonuna dayanmaktadır. Bu yaklaşım, bitki bazlı aşı adaylarının geliştirilmesi için uygulanan karmaşık/pahalı affinite kromatografisine bir alternatif olmaktadır 63.
Mukozal Aşıların ve Bağışıklığı Güçlendirme Planlarının Uygunluğu: Solunum yolu hastalıklarına karşı kullanılan aşıların çoğu parenteral olarak uygulansa da, özellikle burun içi uygulanan mukozal aşılar, patojen etkenlerin girişi için kritik olan akciğerler ve diğer mukozal dokularda solunum yolu hastalıklarına karşı bağışıklığın oluşmasında etkili olmaktadırlar 64,65.
Bazı firmalar, geçici ekspresyon sistemlerini kullanarak bitki bazlı VLP aşılarının üretimine hali hazırda başlamış olsa da, bu çalışmalar esas olarak enjekte edilebilir aşıların geliştirilmesine yönelik olmaktadır 54,66. Bu nedenle mukozal bağışıklama ile ilgili alternatiflerin geliştirilmelidir. Bu amaçla, SARS-CoV-2 antijenlerini kararlı bir şekilde eksprese eden bitkilerin üretilmesi, bu teknolojinin kullanılması için yeni imkanlar sunabilmektedir. Bu yaklaşım ile oral güçlendirici ajanların geliştirilmesine kullanılan SARS-CoV-2 antijenlerini içeren yenilebilir bitki materyalleri üretilmektedir 67. Dondurularak kurutulmuş bitki materyali, termostabilite ve uygulanması kolay özellikleri ile düşük maliyetli bir aşı olarak kullanılmaktadır. Benzer şekilde bitkilerde üretilen saf antijenlerin, geleneksel bir aşının kullanıldığı ve bitkiden elde edilen antijenin takviye amaçlı olarak oral yoldan verildiği uygulamalarda da başarılı olduğu bildirilmiştir 68.
Yenilebilir Aşının Avantajları
Yenilebilir aşının başlıca avantajları şunlardır 36:
1. Bağışıklama için taşıyıcı olarak etkilidir çünkü bağışıklık tepkisini artıran yardımcı maddelere ihtiyaç duyulmamaktadır.
2. Geleneksel aşılarda gözlenmeyen mukozal bağışıklık ortaya çıkmaktadır.
3. Depolama, hazırlama, üretim ve nakliye edilmesinde maliyet açısından etkindir. Biyoteknolojik yöntemle üretilen aşılar, soğuk zincir depolamaya ihtiyaç duyan geleneksel aşıların aksine, aşıları korumak için yıllık maliyeti artıran oda sıcaklığında stabildir. Ayrıca, tohumlarda daha az nem içeriği olduğu için transgenik bitki tohumları kurutulmaktadır. Yağ veya sulu ekstraktlar daha fazla depolama olanağına sahiptir. Yenilebilir aşıların üretimi toprak bakımından zengin bölgelerde kolaylıkla yapılabildiğinden pahalı ekipman ve makinelere ihtiyaç yoktur. Aynı zamanda bitki yetiştirme maliyeti de fermenterlerde yetiştirilen hücre kültürüne göre düşüktür.
4. Bitkilerden üretildiği için kolaylıkla temin edilebilmektedir. Geleneksel aşıların üretiminde gerekli olan özel üretim alanları ve sterilizasyon gibi bölümlere ihtiyaç duyulmadığından üretim maliyeti düşüktür.
5. Geleneksel aşıların aksine enjeksiyon yoluyla uygulama gerektirmediğinden kolaylıkla kabul edilmektedirler. Ayrıca hem sağlık personeli ihtiyacı azalmakta hem de steril koşullara ihtiyaç duyulmadığından dolayı kontaminasyon riski düşük olmaktadır.
6. Bitki türevli aşılar, çok sayıda antijeni birleştiren yeni aşıların kaynağı olabilmektedir. Bu çok bileşenli aşılar, birkaç antijenin aynı anda M hücrelerine yaklaşmasına izin verebildiğinden ikinci nesil aşılar olarak adlandırılmaktadır.
7. Proteinlerin bulaşıcı organizmaya dönüşme olasılığı olmadığından geleneksel aşıya kıyasla bireyin güvenliğini artırmaktadır. Yenilebilir aşılar, zayıflatılmış patojen etkenleri içermezler.
8. Hayvandan üretilme sistemine kıyasla yenilebilir aşının seri olarak üretimi kolay olmaktadır.
Yenilebilir Aşının Dezavantajları
Yenilebilir aşıya ulaşmak kolaydır ancak bazı zorlukları vardır. Yenilebilir aşı kullanımı ile ilgili başlıca sorunlar şunlardır 36:
1. Aşı proteini veya peptidine karşı immüntolerans geliştirme olasılığı bulunmaktadır.
2. Dozaj formunun tutarlılığı, bitki türüne ve nesilden nesile, protein içeriği de hastanın yaşı, ağırlığı, meyvenin olgunluğu ve bitki materyalinin/ürünün standardizasyonu için yöntemler bulunmadığında tüketilen gıdanın miktarına göre farklılık göstermektedir. Yenilebilir aşının düşük dozları tüketildiğinde daha az sayıda antikor üretilmektedir. Buna karşın yüksek dozları ise bağışıklık toleransına neden olmaktadır.
3. Aşı stabilitesi bitkilere göre farklılık göstermektedir.
4. Patates gibi bazı yiyecekler çiğ olarak tüketilemez ve yapısında bulunan proteinin denatüre veya zayıflatacak şekilde pişirilmesine ihtiyaç duyulmaktadır.
5. Yenilebilir aşı için değişen ortam koşulları da büyük bir problemdir. Aşı içeren patatesler 4ºC'de daha uzun süre saklanabilirken domatesler ise bu sıcaklık koşullarında uzun süre muhafaza edilememektedir. Bu nedenle, mikrobiyal bozulma yoluyla enfeksiyonu önlemek için bu aşıların uygun şekilde saklanması gerekmektedir.
6. Toleransa yol açabilecek yanlış aşı uygulamasının önlenmesi amacıyla "aşı meyvesi" ve "normal meyve" arasında uygun ayırt edici karakterlere ihtiyaç duyulmaktadır.
7. Bitkilerin ve insanların glikozilasyon (proteinlere şeker ilavesi) modelleri farklıdır, bu durum aşıların fonksiyonlarını etkileyebilmektedir.