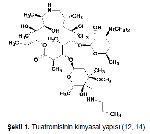
1. Genel Özellikleri
Tulatromisin fermentasyon yoluyla elde edilen yarı sentetik makrolid grubu yeni bir
antimikrobiyel ajandır
1,2. Makrolidler lakton halkasına sahip olduklarından bazik
karakterdedir ve asit ortamda stabil değildir. Lakton halkasındaki karbon atomu sayısına
göre sınıflandırılan makrolidlerden eritromisin ve oleandomisin 14, azitromisin 15,
spiramisin ve tilosin 16 karbon atomuna sahiptir. İlk makrolidler (eritromisin 1952)
eskiden streptomisinden elde edilmelerine rağmen günümüzde artık yarı veya tam
sentetik olarak üretilmektedir.
Kimyasal yapısı: Kimyasal formülü C41H79N3O12, molekül ağırlığı 806.23 g/mol olan
beyaz kristalize bir tozdur. Genellikle tuz ve ester şeklinde bulunur ve kullanılır. İlk çıkan
makrolidlerden yapısında üç adet bazik amino grubunun bulunmasıyla ayrılır. Bu
nedenle kimyasal alt grup triamilid içinde yer almaktadır ve 4. karbon atomundaki
üçüncü amino grubu tulatromisinin bazikliğini artırarak ilaçın hücre membranına penetre
olma yeteneğini artırır3-6. Kimyasal yapısı Şekil 1' de gösterilmiştir.
Tulatromisin izomer A ve B olmak üzere iki izomer karışımını içermektedir. Bu
karışımdaki izomerlerin %90'ı izomer A ve %10'u izomer B halinde bulunmaktadır7-10.
pH değeri ile ilişkisi: İn vitro aktivitesi ortamın pH değerine bağlıdır. Normalde pH 8
veya altında suda iyi çözünebilmektedir11. Minimal inhibe edici konsantrasyon (MIC)
pH 7.0 ve pH 7.0'nin altında (hafif asidik) pH 7.2 - 7.4'ten önemli derecede daha
etkindir. Bu pH fenomeni diğer makrolidler için de geçerlidir. Nötr veya asit pH'da
iyonizasyonla molekülün pozitif yüklenmesi artmakta, böylece yayılma kabiliyeti
azalmakta ve yağdaki çözünürlüğü düşmektedir4,12,13.
Dayanıklılığı: Kimyasal olarak çok stabil olduğundan hazır enjeksiyon sıvıları oda
ısısında 36 ay boyunca saklanabilmektedir. Ayrıca fotostabil (ışığa dayanıklı)
olduğundan renksiz kaplarda paketlenmesine izin verilmiştir1,11.
2. Etki Spektrumu ve Antimikrobiyal Etkinliği
Geniş etki spektrumlu bir ajandır. Genel olarak başta
Gram (+) olmak üzere Gram (-) bakteriler, anaeroblar ve
mikoplazma gibi hücre duvarı olmayan bakterilere karşı
etkilidir (3). İn vitro olarak Mannheimia (Pasteurella)
haemolytica, Pasteurella multocida, Histophilus somni,
Mycoplasma bovis, Actinobacillus pleuropneumoniae,
Mycoplasma hyopneumoniae, Histophilus parasuis'a
karşı etkilidir1.
3. Etki Mekanizması
Hücrede protein sentezi ribozomlarda olur ve protein
sentezinde amino asit dizisine ait şifre çekirdekten
ribozoma taşınan mRNA'daki şifreye göre kodonlarda
gerçekleştirilir. Protein sentezinde önce başlatıcı faktörün
etkisiyle, 70S ribozomu 50S ve 30S alt birimlerine ayrılır,
mRNA bunlardan 30S alt birimine ve tRNA ise başlatıcı
kodona yani 50S alt birimine bağlanır. Sonra alt birimler
birleşerek 70S ribozomu protein sentezine hazır hale
getirilir. Tulatromisinin etki yeri işte bu ribozomal
RNA'ların 50S alt birimidir. Bakterilerde 50S ribozomal alt
birime bağlanıp peptidil tRNA'nın bağlanmasını
engelleyerek peptid zincirinin uzamasını önler ve böylece
protein sentezi engellenir1,3,8,15,16. Genel olarak
bakteriostatik etki göstermesine rağmen, yüksek dozda
Gram (-)'lere karşı bakterisid etki gösterebilmektedir11.
4. Direnç
Makrolidlere karşı direnç hızla gelişebilmektedir.
Direnç, ribozomal RNA'da veya bazı ribozomal
proteinlerde kodlanan genlerdeki mutasyonla;
ribozomlara bağlanma yerinin enzimatik modifikasyonu
(metilasyonu), genellikle linkozamid ile çapraz direnç
oluşumuyla, enzimatik inaktivasyon ile veya aktif bir
pompa sayesinde bakteri hücrelerinde makrolidlerin
dışarı atılması ile gerçekleşmektedir1-3,7,11,12,15,16.
5. Farmakolojik Özellikleri
Emilim ve Dağılımı: 2.5 mg/kg tek doz sığırlara
derialtı ve domuzlara kas içi enjeksiyonu sonrası uygulama yerinden hızlı ve tam olarak emilmektedir.
Vücuda büyük oranda yayıldığı için iyi bir dağılım
göstermektedir1,8,17. Akciğerdeki konsantrasyonu
plazmadaki konsantrasyonundan daha yüksektir. Bu da
akciğerde nötrofil ve alveolar makrofajlar içinde
tulatromisinin biriktiğini göstermektedir1,2,8,11,15.
Fakat akciğerde bulunan enfeksiyon yerinde in vivo
tulatromisin konsantrasyonu tam olarak bilinmemektedir.
Sığırlarda plazma maksimum konsantrasyonu (Cmax)
yaklaşık 0.5 μg/mL, domuzlarda 0.6 μg/mL, maksimum
konsantrasyona ulaşma süresi (tmax) sığır ve domuzlarda
30 dakika, plazma proteinlerine bağlanma oranı %40'dır1. Damar içi uygulama sonrası dağılım hacmi sığırlarda
10-11 L/kg2,10 domuzlarda ise 13.2 L/kg'dır. Sistemik
biyoyararlanımı sığırlarda derialtı uygulamadan sonra
%90, domuzlarda kas içi uygulamadan sonra %88'dir2,3,17.
Akciğer dokusundaki yarılanma ömrü uzundur
(domuzlarda 6 gün, sığırlarda 8 gün). Maksimum
konsantrasyona ulaştıktan sonra vücuttan atılımı oldukça
uzun süre almaktadır. Plazmadaki eliminasyon yarı ömrü
sığırlarda 90 saat, domuzlarda 91 saattir1,8,17.
Metabolizma ve Atılımı: Tulatromisinin
metabolizması çok stabildir12-14. Tüm hayvanlarda
düşük düzeyde metabolize edilir ve esas olarak
değişmemiş ilaç halinde atılır. Aynı şekilde karaciğer ve
safradaki en önemli bileşiği de değişmemiş ilaç
şeklindedir. Hayvan doku numuneleri ve atılma
ürünlerinde metabolitlerin sadece %10'u N-demetilasyon
veya N-oksidasyona uğrayarak metabolize olmaktadır3. Atılımı yavaş fakat tamdır11. Dışkı ve idrarda
ayrıca safra ve insan tüketimine sunulabilen diğer
dokularda genellikle (%90) değişmemiş son ürün olarak
bulunur. Domuzlarda 23 gün içinde uygulanan dozun
yaklaşık 2/3'ü dışkı ve 1/3'ü idrarla atılır. Sığırlarda atılım
biraz daha yavaş olmaktadır. Verilen dozun yaklaşık
%70'i 47 gün içinde atılır, bunun da yaklaşık %40'ı
idrarda, %32'si dışkıda bulunur1,3,8.
6. Endikasyonu
Sığırlarda Mannheimia haemolytica, Pasteurella
multocida, Histophilus somni (Haemophilus somnus),
Actinobacillus pleuropneumonia, Mycoplasma
hyopneumonia ve Mycoplasma bovis'in neden olduğu
solunum sistemi hastalıklarının tedavisi ve korunmasında
kullanılmaktadır2-4,11,12,18-23. İn vitro olarak
tulatromisin, tilmikosine dirençli Pasteurella multocida'ya
etkili Moraxella bovis'in neden olduğu sığırların
enfeksiyoz keratokonjuktivitis'in tedavisinde
kullanılmaktadır24.
Domuzlarda Actinobacillus pleuropneumonia,
Pasteurella multocida ve Mycoplasma hyopneumonia'nin
neden olduğu solunum sistemi hastalıklarının tedavisi ve
korunmasında kullanılmaktadır2-5,12,17,20,25,26.
7. Kullanım Şekli ve Dozu
Genel olarak tulatromisin uygulaması antibiyogram
sonucuna göre yapılır. Sığırlarda deri altı yolla 2.5
mg/kg/canlı ağırlık tek doz olarak uygulanmaktadır. 300 kg'dan daha ağır sığırların tedavisi sırasında doz bir
bölgeye 7.5 mL'den daha fazla uygulanmayacak şekilde
bölünmelidir7. Domuzlarda kas içi 2.5 mg/kg/canlı
ağırlık tek doz olarak uygulanmaktadır3,8,27. 80
kg'dan daha fazla olan domuzların tedavisinde doz bir
bölgeye 2 mL'den fazla uygulanmayacak şekilde
bölünmelidir2. Hayvanlar hastalığın erken safhasında
tedavi edilmeli ve uygulamadan sonraki 48 saat içinde
sonuç değerlendirilmelidir1,7. Solunum yolu
hastalıklarının semptomları hala mevcut ise iyileşinceye
kadar diğer antibiyotiklerle tedavi değişimi tercih
edilmelidir.
8. Yan Etkileri
Lokal yan etki olarak sığırlarda deri altı
uygulanmasını takiben enjeksiyon yerinde 30 güne kadar
kalıcı olabilen şişkinlik ve ağrı oluşabilmektedir. Erişkin
domuzlarda ise kas içi uygulamadan sonra böyle bir
reaksiyon görülmemektedir. Tulatromisin aşırı duyarlılığa
yol açabilmektedir. Gebe hayvanlarda, sütü insan
tüketime sunulan laktasyondaki ineklerde ve süt emen
buzağılarda kullanılmamalıdır2,3,8.
9. İlaç Etkileşimleri
Linkozamid ve kloramfenikol ile aynı anda
uygulanmamalıdır28,29. Her üç ilaçta ribozomlarda
50S alt birime bağlanır. Dolayısı ile bağlı bir antibiyotik
diğerlerinin bağlanma yerini hacimce doldurmaktadır.
Aynı anda uygulama etkinin azalmasına yol açmaktadır.
Makrolidlere karşı duyarlı olan hayvanlarda da
kullanılmamalıdır2,3,7.
10. Toksisitesi
Akut Toksisite: Rat ve köpeklerde yapılan toksisite
çalışmaları tulatromisinin oral yolla tek doz
uygulanmasından sonra hafif, damar içi uygulanmadan
sonra ise orta derecede bir toksisite saptandığını
göstermiştir8. Oral yolla uygulandığında letal doz
köpekte 1000 mg/kg'dan, ratlarda 2000 mg/kg'dan daha
yüksektir. Köpekte 100 mg/kg doz kusma gibi hafif
gastrointestinal bozukluklara neden olmaktadır.
Sığırlarda önerilen dozun 3, 5, 10 misli verilmesinden
sonra enjeksiyon yerinde lokal reaksiyonlara bağlı olarak
geçici huzursuzluk, baş sallama, tepinme ve kısa süreli
iştahsızlık gözlenmektedir. Altı aylık sığırlarda tavsiye
edilen dozun 5-6 misli (12.5-15 mg/kg) uygulanmasıyla
kardiyotoksik etkisine bağlı olarak hafif derecede
miyokardial dejenerasyonların görüldüğü bildirilmiştir1,7. Genç domuzlarda önerilen dozun 3-5 misli
uygulanması halinde enjeksiyon yerindeki lokal reaksiyonlarla ilişkili olarak geçici bağırma ve
huzursuzluk gözlenir. Enjeksiyon arka ekstremitelere
yapılırsa topallıkta gözlenebilmektedir9.
Subkronik ve Kronik Toksisite: Bir ay süresince 10,
50, 200 mg/kg günlük oral tulatromisin uygulaması
ratlarda karaciğer enzimlerinin artışına, karaciğer
ağırlığının azalışına ve monosit ile eozinofillerin artışına
neden olmaktadır. Görülebilir herhangi bir toksik etkiye
yol açmayan en küçük miktar (NOEL) 10 mg/kg/gün'dür.
90 günlük verilim için NOEL 5 mg/kg/gün'dür. Köpekte
oral olarak günlük 5, 10, 15 ve 50 mg/kg' lık doz bir ay
verildikten sonra karaciğer enzimlerinin yükselmesi,
serum proteinlerinin azalması, böbrek ağırlığının artışı ve
sporadik olarak yumuşak dışkı görülür8.
Reprodüksiyona Etkisi: Rat ve tavşanlarda yapılan
laboratuvar çalışmalarında herhangi bir teratojenik etkiye
neden olmadığı gösterilmiştir3,8. Ancak, sığır ve
domuzlarda gebelik ile laktasyon döneminde
uygulanabilirliği tam olarak açıklığa kavuşturulmuş
değildir1,2.
Karsinojen ve Nörotoksik Etki: Tulatromisin
genotoksik, karsinojen veya nörotoksik etki
göstermemektedir8.
İnsan Toksikolojisi: Tulatromisin sadece veteriner
hekimlik için geliştirildiğinden insanlarda toksikolojik
veriler mevcut değildir. Fakat insanlarda kullanılan
azitromisine çok benzemektedir. Toksikolojik kabul
edilebilir günlük alım rat ve köpeklerde 5 mg/kg/gün 90
günlük toksisite çalışmalarının NOEL'ine ve 100 güven
faktörüne göre 0.05 mg/kg/gün olarak
belirlenebilmektedir8.
Gıdalarda Kalıntı Uyarısı: İlaç uygulamasından
sonra 49 gün geçmeden sığırlar kesime sevk
edilmemelidirler2. Sütü insan tüketimine sunulan
laktasyondaki ineklere ve doğumuna 2 aydan az kalan
düve ile ineklere uygulanmamalıdır1,7. Aksi takdirde
besinleri tüketen canlılarda özellikle de insanlarda ilaç
kalıntısının yol açacağı direnç gelişimi görülebilir.
11. Uygulayıcının Alması Gereken Önlemler
Tulatromisinin gözle teması irritasyona neden
olmaktadır2. Bunun sonucunda iriste yangı,
konjuktivitis ve korneada opaklaşma gözlenebilmektedir1. Kaza ile göze temas ederse göz bol miktarda su ile
hemen yıkanmalıdır7. Tulatromisin deri ile teması
duyarlılığa neden olabilir8.